题目内容
16.下列图象与对应实验相符合的是( )| A. | 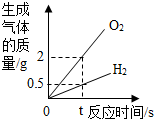 电解水实验 | |
| B. | 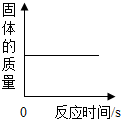 红磷在盛有氧气的密闭容器中燃烧 | |
| C. | 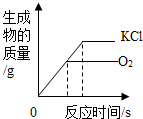 加热一定量的氯酸钾和二氧化锰固体 | |
| D. | 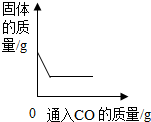 一氧化碳还原一定量氧化铁 |
分析 A、根据水电解时生成的氢气与氧气的质量比分析解答;
B、根据质量守恒定律结合图象反映出的关系相比较,进行判断;
C、根据加热一定量的氯酸钾和二氧化锰固体生成氯化钾和氧气分析即可;
D、根据一氧化碳还原一定量氧化铁会生成一定质量的固体.
解答 解:A、电解水时,生成氢气与氧气的体积比为2:1,质量比为1:8(0.25:2=1:8),故图象错误;
B、根据质量守恒定律可以知道参加反应的固体红磷的质量与氧气的质量之和等于生成的固体五氧化二磷的质量,因此反应后固体的质量增加,故图象错误;
C、加热一定量的氯酸钾和二氧化锰固体生成氯化钾和氧气,相同时间内生成的氯化钾的质量大,且反应停止后氯化钾和氧气同时不再生成,故图象错误;
D、一氧化碳还原一定量氧化铁会生成铁,而且氧化铁的质量是一定的,生成的铁的质量也是一定的,故图象正确.
故选:D.
点评 此题是化学反应与图象知识的考查题,结合反应的过程与图象情况的走势联系起来是解题的关键所在.

练习册系列答案
相关题目
6.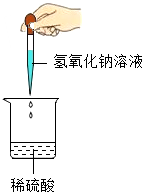 某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想】同学们经过讨论,一致认为溶质一定有硫酸钠,写出该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;
除硫酸钠以外,小明同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)取少量烧杯中溶液于试管中,滴加酚酞试液,无明显现象,据此推断小明同学的猜想不成立,理由是酚酞试液没有变红,溶液中没有氢氧化钠;
(2)取少量烧杯中溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl;
(3)小芳同学提出质疑,因为溶液中硫酸钠与氯化钡反应也会产生白色沉淀,为了证明溶质是否还有硫酸,请你与同学们一起进行如下探究(要求不选指示剂和pH试纸).
【评价与反思】在探究化学反应后的剩余物质的成分时,除了考虑生成物外,还要考虑反应物的用量.
 某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.【提出问题】烧杯内的溶液中溶质是什么?
【猜想】同学们经过讨论,一致认为溶质一定有硫酸钠,写出该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;
除硫酸钠以外,小明同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)取少量烧杯中溶液于试管中,滴加酚酞试液,无明显现象,据此推断小明同学的猜想不成立,理由是酚酞试液没有变红,溶液中没有氢氧化钠;
(2)取少量烧杯中溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl;
(3)小芳同学提出质疑,因为溶液中硫酸钠与氯化钡反应也会产生白色沉淀,为了证明溶质是否还有硫酸,请你与同学们一起进行如下探究(要求不选指示剂和pH试纸).
| 实验步骤 | 实验现象 | 实验结论与解释 |
| 取少量烧杯中溶液于试管中,加入锌(填试剂名称) | 有气泡产生 | 溶质还有硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑ |
11.下列叙述正确的是( )
| A. | 对人体健康而言,铅、镉、汞等是有害元素 | |
| B. | 钙、铁、锌都是人体必需的微量元素 | |
| C. | 人体缺乏维生素A会引起坏血病 | |
| D. | 蛋白质、淀粉、甲烷都是有机高分子化合物 |
1.海水是巨大的资源宝库,利用海水为原料获得许多化工产品的流程如图:
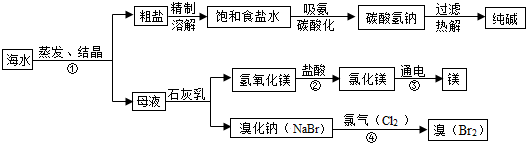
(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、蒸发、计算产率;
(2)步骤①中选用蒸发结晶而不用降温结晶的理由是因为氯化钠的溶解度受温度影响小.
(3)由上述流程图看出碳酸氢钠的热稳定性小于(填“大于、小于或等于)纯碱的热稳定性.
(4)步骤②发生的反应属于复分解反应(填一种基本反应类型).用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有质轻、强度大(任答一点).
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),反应后溴元素的化合价比反应前升高(填“升高”或“降低”或“不变”).
(6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表:
完成下列计算:
①固体样品中氯化钠的质量分数是15.2%;
②第 2 次反应结束后溶液中溶质质量分数是多少?(写出必要的计算题过程)

(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、蒸发、计算产率;
(2)步骤①中选用蒸发结晶而不用降温结晶的理由是因为氯化钠的溶解度受温度影响小.
(3)由上述流程图看出碳酸氢钠的热稳定性小于(填“大于、小于或等于)纯碱的热稳定性.
(4)步骤②发生的反应属于复分解反应(填一种基本反应类型).用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有质轻、强度大(任答一点).
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),反应后溴元素的化合价比反应前升高(填“升高”或“降低”或“不变”).
(6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表:
| 编 号 | 第 1 次 | 第 2次 | 第 3次 |
| 所取固体样品的质量/g | 13 | 10 | 10 |
| 样品用98g水溶解后,加入CaCl2溶液的质量/g | 100 | 100 | 125 |
| 反应后生成沉淀的质量/g | 8 | 8 | 8 |
①固体样品中氯化钠的质量分数是15.2%;
②第 2 次反应结束后溶液中溶质质量分数是多少?(写出必要的计算题过程)
5.某学校化学兴趣小组的同学对我市南部山区的大理石矿区进行调查并取样.样品的主要成分是碳酸钙(其中含有二氧化硅等杂质).下面是同学们的实验探究过程,请你参与并回答有关.
【实验目的】测定大理石样品中碳酸钙的质量分数.
【查阅资料】二氧化硅等杂质不溶于水,也不与盐酸反应.
【实验过程】准确称量5.0g大理石样品于烧杯中,向其中加入40mL质量分数为20%的盐酸,立即将烧杯放在电子秤上称量.每分钟记录一次数据(提示:反应结束后盐酸有剩余).
相关的实验数据如下表:
【数据处理】
(1)表中有一个称量数据是不合理的,该数据的测定时间是5分钟.
(2)计算样品中碳酸钙的质量分数.(写出计算过程,计算结果保留一位小数)
【反思交流】实验结束后,部分同学认为测得的碳酸钙质量分数偏大,请你分析出现此情况的原因可能是烧杯减少的质量除二氧化碳外还含有盐酸挥发出的氯化氢气体.
【实验目的】测定大理石样品中碳酸钙的质量分数.
【查阅资料】二氧化硅等杂质不溶于水,也不与盐酸反应.
【实验过程】准确称量5.0g大理石样品于烧杯中,向其中加入40mL质量分数为20%的盐酸,立即将烧杯放在电子秤上称量.每分钟记录一次数据(提示:反应结束后盐酸有剩余).
相关的实验数据如下表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 102.0 | 101.0 | 100.5 | 100.2 | 100.1 | 100.4 | 100.1 | 100.1 | 100.1 |
(1)表中有一个称量数据是不合理的,该数据的测定时间是5分钟.
(2)计算样品中碳酸钙的质量分数.(写出计算过程,计算结果保留一位小数)
【反思交流】实验结束后,部分同学认为测得的碳酸钙质量分数偏大,请你分析出现此情况的原因可能是烧杯减少的质量除二氧化碳外还含有盐酸挥发出的氯化氢气体.
6.洁净的空气对人类的健康是非常重要的,下列影响空气质量的一组主要污染物是( )
| A. | 二氧化硫 二氧化氮 二氧化碳 | B. | 二氧化硫 二氧化氮 一氧化碳 | ||
| C. | 二氧化碳 氮气 稀有气体 | D. | 一氧化碳 氧气 可吸入颗粒物 |
 、
、 、
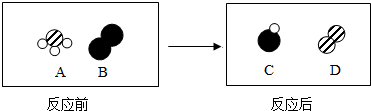
、 各代表三种不同原子,它们形成的分子中A和B反应生成C和D.反应前后分子变化的微观示意图如下所示.请回答:
各代表三种不同原子,它们形成的分子中A和B反应生成C和D.反应前后分子变化的微观示意图如下所示.请回答: