题目内容
7.镁能在二氧化碳中燃烧生成氧化镁和碳.小红据此提出问题:钠能在二氧化碳中燃烧吗?请你与她一起探究这个问题.
(1)提出假设:钠在二氧化碳中燃烧,生成物可能是Na2O、C、Na2CO3、CO.
(2)查阅资料:CO能与氯化钯(PbCl2)溶液反应生成黑色固体钯:CO+PbCl2+H2O═CO2+Pb↓+HCl.
(3)Na2O、Na2CO3均为白色固体.
(4)实验探究:①为了获得干燥的二氧化碳气体,并检查反应的生成物,各装置中合适的试剂,B是浓硫酸,E是氯化钯溶液.取黄豆大小的钠,吸干表面的煤油,放入硬质玻璃管中.
②打开分液漏斗,让稀盐酸滴入平底烧瓶,通入CO2,待出现什么现象时开始点燃酒精灯澄清石灰水变浑浊后.
③钠在加热时能剧烈燃烧,燃烧结束后,硬质玻璃管中有黑色、白色固体生成,E溶液产生黑色沉淀.据此你得出的结论是产物中含有一氧化碳.
④请你设计一个方案探究黑色固体的成分是碳.你的方案是实验步骤:把黑色固体放在氧气中灼烧,把产生的气体通入澄清石灰水中;
实验现象:黑色固体剧烈燃烧,澄清石灰水变浑浊;
实验结论:黑色固体是碳,经检验,白色固体的成分是Na2CO3.
⑤写出钠与CO2加热时的化学反应方程式6Na+5CO2$\frac{\underline{\;\;△\;\;}}{\;}$3Na2CO3+C+CO.
⑥按如图方式连接好装置,若检查气密性.你认为检查该装置气密性的方法是连接装置,把圆底烧瓶浸入热水中,如果BDE装置都产生气泡,说明装置不漏气.
⑦若获得纯净的二氧化碳气体,需除去可能产生的氯化氢气体,你认为应装置AB之间串接一个盛有不与CO2反应的碱性性(填“酸性”或“碱性”)溶液的吸收瓶.
分析 ①浓硫酸可以用来干燥二氧化碳气体;
②澄清石灰水变浑浊后,说明装置中的空气被排出;
③根据实验现象可以判断实验结果;
④碳在氧气中燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊;
⑤根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
⑥凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
⑦碳酸氢钠溶液显碱性,能和氯化氢反应生成氯化钠、水和二氧化碳,不能和二氧化碳反应.
解答 解:①为了获得干燥的二氧化碳气体,并检查反应的生成物,各装置中合适的试剂,B是浓硫酸,用来干燥二氧化碳气体,E是氯化钯溶液,用来检验一氧化碳气体.
故填:浓硫酸;氯化钯溶液.
②打开分液漏斗,让稀盐酸滴入平底烧瓶,澄清石灰水变浑浊后,装置中的空气被完全排出,再通入二氧化碳.
故填:澄清石灰水变浑浊后.
③钠在加热时能剧烈燃烧,燃烧结束后,E溶液产生黑色沉淀,说明生成了一氧化碳,据此得出的结论是产物中含有一氧化碳.
故填:产物中含有一氧化碳.
④探究黑色固体的成分是碳的方案是:实验步骤:把黑色固体放在氧气中灼烧,把产生的气体通入澄清石灰水中;
实验现象:黑色固体剧烈燃烧,澄清石灰水变浑浊;
实验结论:黑色固体是碳.
故填:实验步骤:把黑色固体放在氧气中灼烧,把产生的气体通入澄清石灰水中;
实验现象:黑色固体剧烈燃烧,澄清石灰水变浑浊;
实验结论:黑色固体是碳.
⑤钠与CO2加热时的化学反应方程式为:6Na+5CO2$\frac{\underline{\;\;△\;\;}}{\;}$3Na2CO3+C+CO.
故填:6Na+5CO2$\frac{\underline{\;\;△\;\;}}{\;}$3Na2CO3+C+CO.
⑥按如图方式连接好装置,检查该装置气密性的方法是:连接装置,把圆底烧瓶浸入热水中,如果BDE装置都产生气泡,说明装置不漏气.
故填:连接装置,把圆底烧瓶浸入热水中,如果BDE装置都产生气泡,说明装置不漏气.
⑦若获得纯净的二氧化碳气体,需除去可能产生的氯化氢气体,应装置AB之间串接一个盛有不与CO2反应的显碱性溶液的吸收瓶.
故填:AB;碱性.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. |  焰火表演 | B. |  霓虹灯闪烁 | C. |  音乐喷泉 | D. |  气球腾飞 |
 如图标出的是灭火器的组成物质,请回答下列问题.
如图标出的是灭火器的组成物质,请回答下列问题.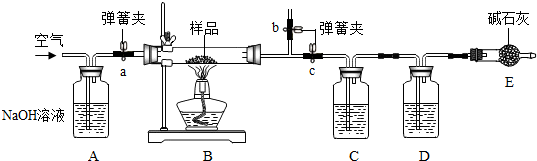
 永春老醋是中国四大名醋之一.它是以优质糯米、红粬、芝麻、水等为原料,用独特配方、精工发酵、陈酿多年而成,具有色泽棕黑、酸中带甘、醇香爽口、久藏不腐等特点,既是质地优良的调味品,又兼有治病妙用,可防治腮腺炎、胆道蛔虫、感冒等疾病.
永春老醋是中国四大名醋之一.它是以优质糯米、红粬、芝麻、水等为原料,用独特配方、精工发酵、陈酿多年而成,具有色泽棕黑、酸中带甘、醇香爽口、久藏不腐等特点,既是质地优良的调味品,又兼有治病妙用,可防治腮腺炎、胆道蛔虫、感冒等疾病.
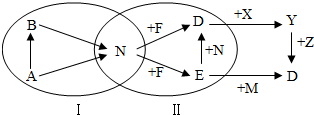 图中用字母表示的10种物质是初中化学常见的物质,N和F都是常见的非金属单质,其余均为化合物,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中的转化均是分解反应,圈Ⅱ中的转化均是化合反应.
图中用字母表示的10种物质是初中化学常见的物质,N和F都是常见的非金属单质,其余均为化合物,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中的转化均是分解反应,圈Ⅱ中的转化均是化合反应.