题目内容
17.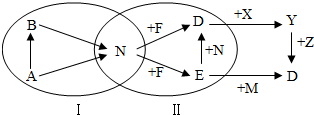 图中用字母表示的10种物质是初中化学常见的物质,N和F都是常见的非金属单质,其余均为化合物,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中的转化均是分解反应,圈Ⅱ中的转化均是化合反应.
图中用字母表示的10种物质是初中化学常见的物质,N和F都是常见的非金属单质,其余均为化合物,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中的转化均是分解反应,圈Ⅱ中的转化均是化合反应.(1)N在空气中体积分数约占$\frac{1}{5}$,则N的化学式为O2;若X、Y、Z的类别不同,则Y的类别为盐.(选填酸、碱、盐、有机物)
(2)请写出E+N→D反应的化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
(3)若M在变化前后由红色变为黑色,写出符合此现象E+M→D的化学反应方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 N在空气中体积分数约占$\frac{1}{5}$,则N为氧气;由制取氧气的方法以及图中A、B、N三种物质的转化关系可知A为双氧水,B为水,双氧水分解生成氧气和水,水电解生成氧气,故N为氧气;F是非金属单质且与氧气反应生成不同的物质,故F为碳,碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳;一氧化碳燃烧能生成二氧化碳,故E为一氧化碳,D为二氧化碳,D二氧化碳能与碱溶液反应生成碳酸盐,碳酸盐与酸反应能生成二氧化碳,故X为碱,Y为盐,Z为酸.
解答 解:N在空气中体积分数约占$\frac{1}{5}$,则N为氧气;由制取氧气的方法以及图中A、B、N三种物质的转化关系可知A为双氧水,B为水,双氧水分解生成氧气和水,水电解生成氧气;F是非金属单质且与氧气反应生成不同的物质,故F为碳,碳充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳;一氧化碳燃烧能生成二氧化碳,故E为一氧化碳,D为二氧化碳,D二氧化碳能与碱溶液反应生成碳酸盐,碳酸盐与酸反应能生成二氧化碳,故X为碱,Y为盐,Z为酸.
(1)由上述分析可知N为氧气,化学式为,Y为盐
(2)E为二氧化碳,D为二氧化碳,一氧化碳燃烧生成二氧化碳,化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(3)M在变化前后由红色变为黑色,则M为氧化铁,一氧化碳还原氧化铁生成黑色的铁粉,化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
故答案为:(1)O2;盐;
(2)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
| A. | 该反应生成物中有单质 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后分子数目没有发生改变 | |
| D. | 反应前甲、乙两种分子的个数比是1:2 |
| A. | 滴水成冰 | B. | 水落石出 | C. | 百炼成钢 | D. | 木已成舟 |
| A | B | C | D | |
| 实验要求 | 除去二氧化碳中 少量的氧气 | 清洗金属 表面油污 | 检验生石灰中 是否含有石灰石 | 除去一氧化碳中少量的二氧化碳 |
| 第一方案 | 通过灼热炭粉 | 稀硫酸洗涤 | 滴加醋酸 | 通过灼热的Fe2O3粉末 |
| 第二方案 | 通过灼热铜丝网 | 用洗洁精洗涤 | 加热 | 通过氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 合金:生铁、赤铜、青铜 | |
| B. | 有机物:甲烷、酒精、葡萄糖 | |
| C. | 纯净物:冰水混合物、纯碱、98%浓硫酸 | |
| D. | 氧化物:双氧水、生石灰、烧碱 |

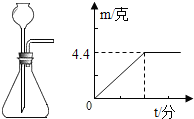 小明用如图发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.
小明用如图发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.