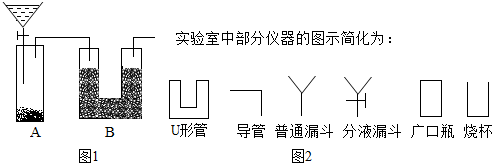
题目内容
3.下列各组物质在pH=14的某无色溶液中,能大量共存的是( )| A. | FeCl3 NaCl KNO3 | B. | NaCl NaOH NaNO3 | ||
| C. | CaCl2 NaNO3 Na2CO3 | D. | KNO3 H2SO4 NaCl |
分析 pH为14的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存,还要注意能得到无色溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为14的水溶液显碱性,水溶液中含有大量的OH-.
A、FeCl3溶液的铁离子和碱性溶液中的中OH-在溶液中结合生成氢氧化铁沉淀,不能大量共存,且FeCl3溶液为黄色,故选项错误;
B、三者在溶液中相互交换成分不能生成沉淀、气体、水,能在溶液中大量共存,且都是无色的,故选项正确;
C、Na2CO3和CaCl2在溶液中能相互交换成分生成碳酸钙沉淀和氯化钠,不能大量共存,故选项错误;
D、H2SO4中的氢离子和碱性溶液中的中OH-在溶液中结合生成水,不能大量共存,故选项错误;
故选B.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水,还要注意是在pH=14的溶液中共存及特定离子的颜色.

练习册系列答案
相关题目
14.将待提纯的物质中杂质(括号内为杂质)除去,所用试剂和方法均正确的是( )
| 选项 | 待提纯物质 | 选用试剂 | 操作方法 |
| A | CuCl2(FeCl2) | 铁粉 | 过滤、洗涤 |
| B | CaO(CaCO3) | 盐酸 | 蒸发、结晶 |
| C | Cu(CuO) | 稀硫酸 | 过滤、洗涤、干燥 |
| D | MnO2(KCl) | 水 | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
11.下列物品所使用的主要材料为有机合成材料的是( )
| A. |  塑料玩具 | B. |  纯棉帽子 | C. |  陶瓷餐具 | D. |  钻石戒指 |
18.下列关于物质用途的叙述,易造成重大伤亡事故的是( )
| A. | 活性炭可做冰箱除臭剂 | B. | 庆典活动可使用大量氢气球 | ||
| C. | 熟石灰可用来粉墙 | D. | 钛合金可做轮船外壳 |
8.观察和实验是学习化学的重要方式,下列实验中观察到的颜色不正确的是( )
| A. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 加热碱式碳酸铜观察到固体由绿色变为黑色 | |
| C. | 无水硫酸铜粉末遇水固体会由蓝色变为白色 | |
| D. | 氢氧化钠溶液中滴加硫酸铜溶液生成蓝色沉淀 |
13.铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
(1)恰好反应时的实验现象是剩余金属表面没有气泡产生.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
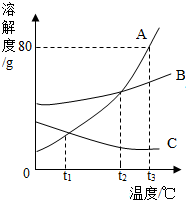 如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答:
如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答: