题目内容
13.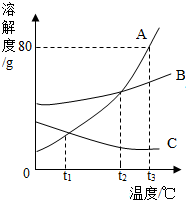 如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答:
如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答:(1)用S表示物质的溶解度,在t2℃时,SA=SB>SC.
(2)随着温度的升高,A、B、C三种物质的饱和溶液中有溶质从溶液中析出的是C.
(3)要将B物质从它的饱和溶液中析出,应采用的方法是蒸发(填“冷却”或“蒸发”)结晶法.
(4)t3℃时,50g水中加入50g A物质,可形成饱和溶液(填“饱和”或“不饱和”),该溶液的溶质质量分数为44.4%.
分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;用S表示物质的溶解度,在t2℃时,SA=SB>SC;随着温度的升高,A、B、C三种物质的饱和溶液中有溶质从溶液中析出的是C,因为C的溶解度随温度的升高而减少;要将B物质从它的饱和溶液中析出,应采用的方法是蒸发结晶法,因为B的溶解度受温度的影响很小;t3℃时,A溶解度是80g,因此50g水中加入50g A物质,可形成饱和溶液;该溶液的溶质质量分数=$\frac{40g}{90g}×100%≈44.4%$.
解答 解:(1)由溶解度曲线可知:用S表示物质的溶解度,在t2℃时,SA=SB>SC;故答案为:t2
(2)随着温度的升高,A、B、C三种物质的饱和溶液中有溶质从溶液中析出的是C,因为C的溶解度随温度的升高而减少;故答案为:C
(3)要将B物质从它的饱和溶液中析出,应采用的方法是蒸发结晶法,因为B的溶解度受温度的影响很小;故答案为:蒸发
(4)t3℃时,A溶解度是80g,因此50g水中加入50g A物质,可形成饱和溶液;该溶液的溶质质量分数=$\frac{40g}{90g}×100%≈44.4%$;故答案为:饱和;44.4%;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
2.生活中一些食品或用品的近似PH如表,以下说法做法正确的是( )
| 食品或用品 | 厕所清洁剂 | 泡 菜 | 牙 膏 | 草木灰 |
| pH | 1~2 | 3~4 | 8~9 | 10~11 |
| A. | 用铝制容器盛放厕所清洁剂 | B. | 草木灰可以降低土壤碱性 | ||
| C. | 胃酸过多的人不宜吃泡菜 | D. | 测溶液酸碱度时,pH试纸应润湿 |
3.下列变化过程中没有发生化学变化的是( )
| A. | 粮食酿酒 | B. | 石灰浆抹墙 | ||
| C. | 菜刀生锈 | D. | 晾干的咸菜表面出现白色晶体 |
8.通过查阅资料得知:将熟石灰与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.为了制取氢氧化钾,兴趣小组的同学将少量熟石灰放入烧杯中,再向其中加入一定量碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示,请你与小组同学共同完成以下探究:
【提出问题1】固体A中的成分是什么?
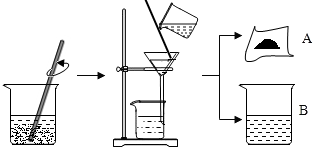
【猜想与假设】甲同学:只有CaCO3; 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
【反思与评价】小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是有气泡生成说明了含有碳酸钙,不能说明含有氢氧化钙;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3;丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是固体中含有氢氧化钙,说明了溶液为氢氧化钙的饱和溶液,溶液中含有氢氧化钙.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
【提出问题1】固体A中的成分是什么?

【猜想与假设】甲同学:只有CaCO3; 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 猜想正确 反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加无色酚酞试液 | 溶液由无色变为红色 | 猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3;丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是固体中含有氢氧化钙,说明了溶液为氢氧化钙的饱和溶液,溶液中含有氢氧化钙.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
5.下列认识正确的是( )
| A. | 聚乙烯和聚氯乙烯都可以包装食品 | |
| B. | 红磷在空气中燃烧产生大量的白烟 | |
| C. | 普通玻璃和有机玻璃都属于无机非金属材料 | |
| D. | 铁加入稀硫酸中得到黄色溶液 |
2. 通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.
通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.
(1)请从C、H、N、O四种元素中选择一种或几种元素,写出符合下列要求的化学式.
①空气中含量最多的气体N2 ②用于炼铁的气体CO
③最常用的溶剂H2O ④能做消毒剂的有机物H2O2
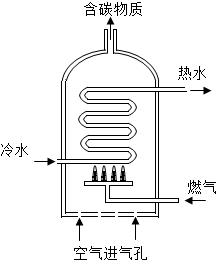
(2)右图是某种燃气热水器的示意图.
①某热水器是以天然气为燃气,天然气的主要成分
是CH4,当“空气进气孔”被部分堵塞,燃
烧时容易产生有毒气体 M,M的化学式为CO.
②1kg不同燃料燃烧产生CO2和SO2的质量如表.根据数据可知,污染最少的燃料是天然气,燃烧生成的SO2容易产生的环境问题是酸雨.
 通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.
通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.(1)请从C、H、N、O四种元素中选择一种或几种元素,写出符合下列要求的化学式.
①空气中含量最多的气体N2 ②用于炼铁的气体CO
③最常用的溶剂H2O ④能做消毒剂的有机物H2O2
(2)右图是某种燃气热水器的示意图.
①某热水器是以天然气为燃气,天然气的主要成分
是CH4,当“空气进气孔”被部分堵塞,燃
烧时容易产生有毒气体 M,M的化学式为CO.
②1kg不同燃料燃烧产生CO2和SO2的质量如表.根据数据可知,污染最少的燃料是天然气,燃烧生成的SO2容易产生的环境问题是酸雨.
| 燃料 | 相关燃烧产物的质量/g | |
| CO2 | SO2 | |
| 汽油 | 2900 | 5.0 |
| 天然气 | 2500 | 0.1 |
| 煤 | 2500 | 11.0 |
3.下列各组物质在pH=14的某无色溶液中,能大量共存的是( )
| A. | FeCl3 NaCl KNO3 | B. | NaCl NaOH NaNO3 | ||
| C. | CaCl2 NaNO3 Na2CO3 | D. | KNO3 H2SO4 NaCl |
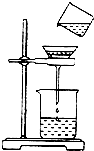 如图是明明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,进行过滤的操作.
如图是明明同学将浑浊的河水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿,进行过滤的操作. 南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.
南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.