题目内容
19.在做盐跟盐反应的分组实验时,第一组学生进行BaCl2与Na2CO3溶液的反应,第二组学生进行BaCl2与Na2SO4溶液的反应.实验结束后,两组同学将全部的浊液集中倒进一个废液缸中.浊液中白色沉淀物质是碳酸钡和硫酸钡.化学兴趣小组对浊液进行过滤,探究滤液的成.
【提出问题】滤液里除了H2O和NaCl外,还有什么物质
【提出猜想】猜想①:Na2CO3
猜想②:Na2SO4
猜想③:Na2CO3、Na2SO4
猜想④:BaCl2
【实验探究】

(1)若“现象a”只有白色沉淀,则猜想④成立;若“现象a”只有气泡产生,则猜想①③可能成立.
(2)若“现象b”产生白色沉淀,然后加入过量稀硝酸,如果沉淀部分溶解并产生气泡,则猜想③成立;如果加入过量稀硝酸,沉淀全部不溶解,则产生该不溶沉淀的反应方程式为BaCl2+Na2SO4═BaSO4↓+2NaCl.
分析 氯化钡和碳酸钠反应能够生成碳酸钡沉淀和氯化钠,和硫酸钠反应能够生成硫酸钡沉淀和氯化钠;
当氯化钡过量时,滤液中含有氯化钠和氯化钡;当碳酸钠过量时,滤液中含有氯化钠和碳酸钠;当硫酸钠过量时,滤液中含有硫酸钠;当碳酸钠、硫酸钠都过量时,滤液中含有氯化钠、碳酸钠和硫酸钠;
根据实验现象可以判断滤液中溶质的存在情况.
解答 解:氯化钡和碳酸钠反应能够生成碳酸钡沉淀和氯化钠,和硫酸钠反应能够生成硫酸钡沉淀和氯化钠,浊液中白色沉淀物质是碳酸钡和硫酸钡.
故填:碳酸钡;硫酸钡.
[提出猜想]
当氯化钡过量时,滤液中含有氯化钠和氯化钡;当碳酸钠过量时,滤液中含有氯化钠和碳酸钠;当硫酸钠过量时,滤液中含有硫酸钠;当碳酸钠、硫酸钠都过量时,滤液中含有氯化钠、碳酸钠和硫酸钠,滤液里除了NaCl外,还可能含有氯化钡,或硫酸钠,或碳酸钠,或碳酸钠和硫酸钠.
故填:BaCl2;
[实验探究]
若现象a只有白色沉淀,则滤液中含有氯化钠和氯化钡.
故填:④.
若现象a只有气泡产生,则滤液中含有氯化钠和碳酸钠,或含有氯化钠、碳酸钠和硫酸钠.
故填:①③.
(2)若现象b产生白色沉淀,然后加稀硝酸沉淀部分溶解,并产生气泡,说明滤液中含有氯化钠、碳酸钠和硫酸钠,因为氯化钡和碳酸钠反应生成的碳酸钡沉淀能够和稀硝酸反应,而氯化钡和硫酸钠反应生成的硫酸钡,不能和稀硝酸反应.
故填:③.
若沉淀全部不溶解,则滤液中含有氯化钠和硫酸钠,硫酸钠与氯化钡反应生成的硫酸钡和盐酸,化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
故填:BaCl2+Na2SO4═BaSO4↓+2NaCl.
点评 实验现象明显、直观,可以帮助我们更好地理解反应过程,因此要注意观察实验现象,学会分析实验现象,从而进行正确的判断.

练习册系列答案
相关题目
10.速效感冒冲剂的主要成分之一是“对乙酰氨基酚”,其化学式为C8H9NO2,有关它的叙述错误的是( )
| A. | “对乙酰氨基酚”由碳、氢、氮、氧四种元素组成 | |
| B. | 一个“对乙酰氨基酚”分子中只有2个氧原子 | |
| C. | “对乙酰氨基酚”分子中碳、氢、氮、氧原子质量比是8:9:1:2 | |
| D. | “对乙酰氨基酚”中碳元素的质量分数约为63.6% |
7.一定质量某硝酸钾样品中不含可溶性杂质.在10℃时加蒸馏水使之充分溶解,残留固体的质量为250g.若该实验在40℃下进行时,残留固体质量为120g;70℃时为20g.已知KNO3在不同温度下的溶解度如下.对该样品的推断正确的是( )
| 温度/℃ | 10 | 40 | 55 | 70 |
| 溶解度/g | 20 | 65 | 100 | 140 |
| A. | 该硝酸钾样品为纯净物 | B. | 40℃时溶于水的硝酸钾为130g | ||
| C. | 70℃时KNO3溶液为饱和溶液 | D. | 55℃左右时KNO3完全溶解 |
14.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某化学课外兴趣小组对生成物中碳的氧化物种类进行了如表实验探究:
提出问题:生成物中有哪几种碳的氧化物?
猜测:
设计实验:基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如图实验:
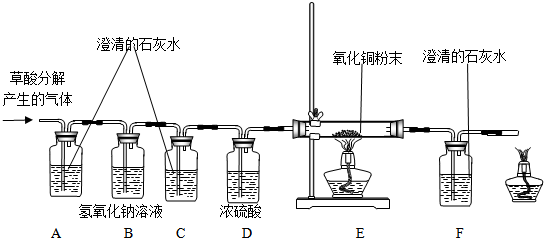
实验探究:
(1)观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现黑色粉末变成红色粉末的现象.
实验结论:通过实验探究证明:猜测3成立.草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O.
问题讨论:
(1)B装置中的作用除去混合气体中的二氧化碳气体;D装置的作用是除去气体中的水蒸汽.
(2)装置末端酒精灯的作用是除去CO气体防止污染空气.
提出问题:生成物中有哪几种碳的氧化物?
猜测:
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |

实验探究:
(1)观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现黑色粉末变成红色粉末的现象.
实验结论:通过实验探究证明:猜测3成立.草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O.
问题讨论:
(1)B装置中的作用除去混合气体中的二氧化碳气体;D装置的作用是除去气体中的水蒸汽.
(2)装置末端酒精灯的作用是除去CO气体防止污染空气.
11.下列概念中,前者属于后者的是( )
| A. | 氧化物、纯净物 | B. | 单质、化合物 | C. | 化合物、混合物 | D. | 纯净物、单质 |