题目内容
4.分类法是化学学习和研究的重要方法之一,下列分类正确的是( )| A. | 盐:小苏打、硫酸铜、硝酸铵 | B. | 无机物:H2O、CaCO3、C2H3OH | ||
| C. | 混合物:冰水共存物、石油、熟石灰 | D. | 合成材料:塑料、合成纤维、合金 |
分析 A.根据盐的概念来分析;
B.根据无机物的概念来分析;
C.根据混合物的概念来分析;
D.根据合成材料的分类来分析.
解答 解:A.小苏打是由钠离子和碳酸氢根离子构成的化合物,硫酸铜是由铜离子和硫酸根离子构成的化合物,硝酸铵是由铵根离子和硝酸根离子构成的化合物,均属于盐,故正确;
B.H2O中不含碳元素,属于无机物,CaCO3虽然含有碳元素,但仍然属于无机物,C2H3OH是一种含碳元素的化合物,属于有机物,故错误;
C.冰水混合物中只含水这一种物质,属于纯净物,故错误;
D.合成材料包括塑料、合成纤维和合成橡胶,合金属于金属材料,故错误.
故选A.
点评 解答本题关键是要知道混合物、盐、合成材料的概念,熟悉无机物与有机物的判断方法.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
16.大多数不粘锅的内壁上都涂有一层聚四氟乙烯的涂层,其化学式可以表示为(CF2CF2)m(m为正整数).下列关于聚四乙烯的说法正确的是( )
| A. | 该物质是一种遇热不稳定的有机化合物 | |
| B. | 该物质受热后易发生化学变化 | |
| C. | 该物质的相对分子质量为100 | |
| D. | 该物质含氟的质量分数为76% |
13.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | HCl | 依次通过足量的NaOH溶液和浓硫酸 |
| B | FeSO4溶液 | CuSO4 | 加入足量的锌粒,充分反应,过滤 |
| C | NaCl溶液 | Na2CO3 | 加入适量的澄清石灰水,过滤 |
| D | KCl | MnO2 | 加水充分溶解,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
14.某兴趣小组同学对碱式碳酸铜的分解产物进行探究.
【查阅资料】
①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
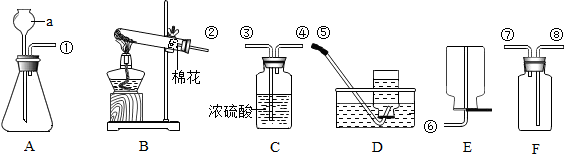
【实验验证】验证碱式碳酸铜的分解产物,可选装置如图所示.

(1)A中的药品是澄清石灰水.
(2)甲同学将装置按BCA(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
【拓展探究】
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分.
【猜想】
猜想Ⅰ是Cu2O(氧化亚铜,红色固体)
猜想Ⅱ是铜;
猜想Ⅲ是铜和氧化亚铜的混合物
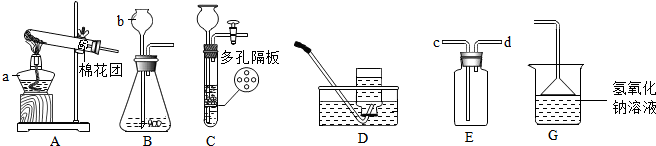
【实验探究】实验装置如图

(1)实验过程
打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
(3)实验结论
通过实验中获得的数据进行计算,猜想Ⅲ(填“Ⅰ”、“Ⅱ”、“Ⅲ”)正确.
【查阅资料】
①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】验证碱式碳酸铜的分解产物,可选装置如图所示.

(1)A中的药品是澄清石灰水.
(2)甲同学将装置按BCA(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,振荡 | 固体完全溶解,溶液变蓝 | 黑色粉末均为氧化铜 | CuO+H2SO4=CuSO4+H2O |
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分.
【猜想】
猜想Ⅰ是Cu2O(氧化亚铜,红色固体)
猜想Ⅱ是铜;
猜想Ⅲ是铜和氧化亚铜的混合物
【实验探究】实验装置如图

(1)实验过程
打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7g |
| 玻璃管的质量为60.0g | |
通过实验中获得的数据进行计算,猜想Ⅲ(填“Ⅰ”、“Ⅱ”、“Ⅲ”)正确.