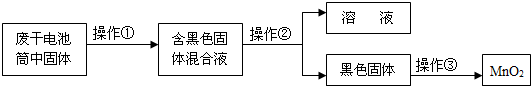
题目内容
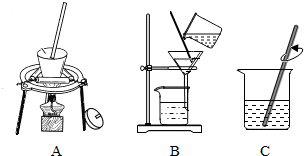
7.根据如图回答问题.
(1)仪器a的名称是试管.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;选用的发生装置为B.
(3)实验室制取二氧化碳的收集装置为C;验满方法为将燃着木条放在集气瓶口,熄灭,二氧化碳收集满.
分析 (1)依据实验室常用仪器的认识解决此题.
(2)书写化学式应该注意化学式、配平、条件、箭头;利用高锰酸钾制氧气是固体加热,装置是A;
(3)实验室制取二氧化碳是用大理石与稀盐酸反应,写出化学方程式,据二氧化碳密度比空气大,溶于水且与水反应选择收集装置,据二氧化碳的检验方法解答此题.
解答 解:(1)仪器a的名称是试管;
(2)高锰酸钾加热生成锰酸钾、二氧化锰、氧气,故反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;利用高锰酸钾制氧气是固体加热,发生装置是B;
(3)根据二氧化碳密度比空气大,溶于水且与水反应,选择收集装置为C,二氧化碳的检验方法是:将燃着的木条放到集气瓶口,若木条熄灭,说明收集满.
故答案为:
(1)试管;(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑; B;
(3)C;将燃着木条放在集气瓶口,熄灭,二氧化碳收集满.
点评 熟练掌握实验室中制取气体的发生装置和收集装置的选择依据,并能作出正确的选择,记住常见气体制取的反应原理,并能够正确书写化学方程式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列用品所使用的主要材料,属于天然纤维的是( )
| A. |  橡胶轮胎 | B. |  尼龙丝袜 | C. |  塑料饭盒 | D. |  羊毛毛衣 |
12.下列食物富含糖类的是( )
| A. | 米饭 | B. | 黄瓜 | C. | 牛肉 | D. | 植物油 |
4.分类法是化学学习和研究的重要方法之一,下列分类正确的是( )
| A. | 盐:小苏打、硫酸铜、硝酸铵 | B. | 无机物:H2O、CaCO3、C2H3OH | ||
| C. | 混合物:冰水共存物、石油、熟石灰 | D. | 合成材料:塑料、合成纤维、合金 |

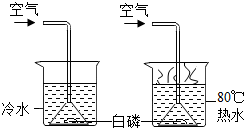 小强用如图所示装置进行实验,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧.
小强用如图所示装置进行实验,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧. 小萌和爸爸一起打扫客厅.
小萌和爸爸一起打扫客厅.