��Ŀ����
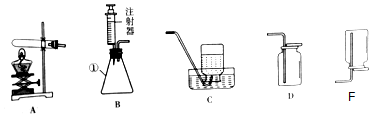
8���������г��л�ѧʵ�鿼��������ǡ�ʵ������ȡ������̼���塱��ͼ1��ʵ�����Ʊ����������װ��ʾ��ͼ��
��1��ʵ�����Ʊ�CO2�Ļ�ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2�������õķ���װ���У�BCDEF��ѡ����ͼ��ĸ��ţ���
��2��װ��E��F�����װ��C�ڲ������������Ϊ�����Կ��Ʒ�Ӧ�ķ�����ֹͣ��
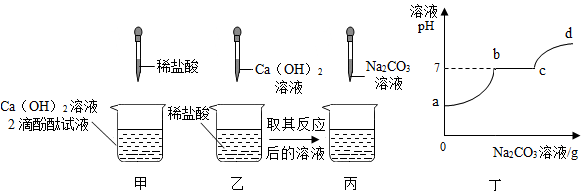
��3��ʵ�����ó���ʯ��ˮ���������̼�Ĵ��ڣ��÷�Ӧ�Ļ�ѧ����ʽΪCO2+Ca��OH��2�TCaCO3��+H2O����������̼������������̼�ֻ���̼��ơ�ˮ��Ӧ����������ˮ��̼�����[Ca��HCO3��2]���ɴ˿����Ƴ���Ӧ�������ͬ����������ܲ�ͬ��
��4��ͼ2��С�����CO2��ȡ���ռ�����������Ҫ�������̣�������Ҫ��������D��ѡ��ͼ2��ĸ��ţ�����ȷ�IJ���Ӧ�ø�Ϊ��ȼ�ŵ�ľ�����ڼ���ƿ�ڣ�

��5����ͼ3��ʾ����CO2���Թ��ڵ���һ�����ij���ʯ��ˮ�������������ϡ��³�����һ��ʱ�䣮����˵����ȷ����ACD��ѡ����ĸ��
A����������Լ����֮һ�����Թܿ�
B���Թ���ѹǿ�����Թ������ѹǿ
C���п��ܻ����ʯ��ˮ�ȱ���Ǻ��ֱ���������
D������������Ŀ����Ϊ�˷�ֹʯ��ˮ����Թܸ�ʴƤ����ͬʱҲ�ٽ���ʯ��ˮ�������CO2
��6����֪����̼��������Һ�������ն�����̼�е��Ȼ������壬Ϊ�˵õ�����������Ķ�����̼���壬����װ�ã���ͼ4��ʾ���ĵ��ܰ�������������˳����C��ѡ����ĸ��
A��c��b��c��d
B��b��a��c��d
C��c��d��a��b
D��d��c��b��a
��7����ʵ������ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼������װ����ͼ5��ʾ���ٴ�ֹˮ�У�������ϡ����δ�����п����ϰ��ϵ�ʯ��ʯ�Ӵ�������ʱ����ϡ����ɼӣ���������Һ�У������˴ӳ���©�������ӵ���C��ѡ����ĸ��
A������������Һ B��̼������Һ
C����������Һ D������ʯ��ˮ
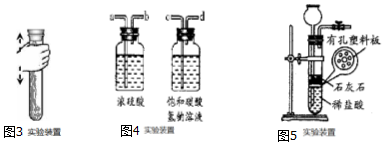
���� ��1������̼��ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼���÷�Ӧ�ķ�Ӧ�ǹ����Һ�壬��Ӧ�����dz��½��з�����
��2������װ��E��Fͨ��װ����ѹǿ�ĸı����ʵ�ֹ����Һ��ķ�����з�����
��3�����ݶ�����̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ���з�����
��4�����ݼ��װ�������ԣ��㵹Һ�壬��ȡ���ռ����壬������̼��������ȷ�������з�����
��5�����ݶ�����̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ���з�����
��6�����ݱ���̼�����ƿ��������Ȼ��⣬Ũ��������ˮ�ԣ�ϴ��Ӧ�ó����̳����з�����
��7�����ݼ�������ʲ��ܺ����ᷴӦ���з�����
��� �⣺��1��̼��ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2�����÷�Ӧ�ķ�Ӧ�ǹ����Һ�壬��Ӧ�����dz��£����Կ��õķ���װ���У�BCDEF��
��2��װ��E��Fͨ��װ����ѹǿ�ĸı����ʵ�ֹ����Һ��ķ��룬���������װ��C�ڲ������������Ϊ�����Կ��Ʒ�Ӧ�ķ�����ֹͣ��
��3��������̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ����ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��������̼������������̼�ֻ���̼��ơ�ˮ��Ӧ����������ˮ��̼�����[Ca��HCO3��2]���ɴ˿����Ƴ���Ӧ�������ͬ����������ܲ�ͬ��
��4��A�����װ��������ʱ���Ƚ�����һ������ˮ�У����ֽ����Թ���ڣ����ܿ������ݲ�����֤��װ�����������ã�����ȷ��
B���㵹Һ��ʱ��ƿ�����ţ��Թ���б����ǩ�������ģ�����ȷ��
C����ȡ����ʱ������Ӧ�����뼯��ƿ�ײ�������ȷ��
D������ʱ��ȼ�ŵ�ľ��Ӧ�÷��ڼ���ƿ�ڣ��ʴ���
��ѡ��D��
��5��A����������Լ����֮һ�����Թܿڣ�����ȷ��
B��������̼���������Ʒ�Ӧ����̼��Ƴ�����ˮ���Թ���ѹǿС���Թ������ѹǿ���ʴ���
C��������̼����ʱ��Ҳ���ܻ���̼��ơ�ˮ��Ӧ��������ˮ��̼����ƣ��п��ܻ����ʯ��ˮ�ȱ���Ǻ��ֱ�����������ȷ��
D������������Ŀ����Ϊ�˷�ֹʯ��ˮ����Թܸ�ʴƤ����ͬʱҲ�ٽ���ʯ��ˮ������ն�����̼������ȷ��
��ѡ��ACD��
��6������̼�����ƿ��������Ȼ��⣬Ũ��������ˮ�ԣ�ϴ��Ӧ�ó����̳������Գ���װ�õĵ��ܰ�������������˳���ǣ�c��d��a��b����ѡ��C��
��7����������ʲ��ܺ����ᷴӦ���������ƻ������ᷴӦ�����Ȼ��ƣ�̼���ƻ������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����������Ҳ�������ᷴӦ����ѡ��C��
�ʴ�Ϊ����1��CaCO3+2HCl�TCaCl2+CO2��+H2O��BCDEF��
��2�����Կ��Ʒ�Ӧ�ķ�����ֹͣ��
��3��CO2+Ca��OH��2�TCaCO3��+H2O����Ӧ�������
��4��D����ȼ�ŵ�ľ�����ڼ���ƿ�ڣ�
��5��ACD��
��6��C��
��7��C��
���� ������Ҫ���鳣������ķ���װ�����ռ�װ�õ�̽��������װ�����ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ���ռ�װ������������ܶȺ��ܽ���ѡ��

 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�| A�� | ���٢� | B�� | �ۢ� | C�� | �٢� | D�� | �ڢ� |
| A�� | Na2CO3��NaCl | B�� | KCl��Fe��NO3��3 | C�� | H2SO4��BaCl2 | D�� | KNO3��CuSO4 |
��NH3+H2O+CO2�TNH4HCO3
��NaCl�����ͣ�+NH4HCO3�TNH4C1+NaHCO3��
��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
����˵����ȷ���ǣ�������
| A�� | �ڷ�Ӧ�Ǹ��ֽⷴӦ | |
| B�� | �۷�Ӧ������̼Ԫ�صĻ��ϼ۷����˸ı� | |
| C�� | �۷�Ӧ���H2O��CO2���Ա�ѭ��ʹ�� | |
| D�� | ��Ӧ������ֻ�õ�һ�ֲ���Na2CO3 |
| A�� |  ʵ������ȡ������̼ | B�� |  ���Թ��еμ���Һ | ||
| C�� |  ���װ�õ������� | D�� |  ʵ������ȡ���� |
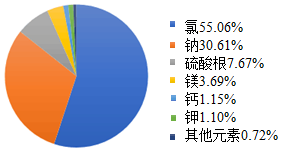 �����к���ʮ������ǧ��������ǧ��ˮ��Լռ��������ˮ����97%����ˮ��������ʵ��Һ���أ�ƽ��ÿ��������ĺ�ˮ����3570��ֵĿ����ʣ���������֪��100����Ԫ���У�80%�����ں�ˮ���ҵ�����ͼΪ��ˮ���ܽ���ηֱ�����ˮ����½���ϵ�ˮ����Դ������ĵ����������纣��ÿ�������ĵ�ˮ��450�������������90%ͨ�����귵�غ���10%��Ϊ��ѩ���ڴ���ϣ�Ȼ��˳�����ַ��غ���ˮ�����������ڷ�չ��Ϊ��ҵ������Ԥ�ƣ�������̬�����Ķ�������ˮ�ĵ����;���ܿ����ǶԺ�ˮ�ĵ�����
�����к���ʮ������ǧ��������ǧ��ˮ��Լռ��������ˮ����97%����ˮ��������ʵ��Һ���أ�ƽ��ÿ��������ĺ�ˮ����3570��ֵĿ����ʣ���������֪��100����Ԫ���У�80%�����ں�ˮ���ҵ�����ͼΪ��ˮ���ܽ���ηֱ�����ˮ����½���ϵ�ˮ����Դ������ĵ����������纣��ÿ�������ĵ�ˮ��450�������������90%ͨ�����귵�غ���10%��Ϊ��ѩ���ڴ���ϣ�Ȼ��˳�����ַ��غ���ˮ�����������ڷ�չ��Ϊ��ҵ������Ԥ�ƣ�������̬�����Ķ�������ˮ�ĵ����;���ܿ����ǶԺ�ˮ�ĵ�����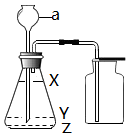 ��ѧ��һ����ʵ��Ϊ������ѧ�ƣ�
��ѧ��һ����ʵ��Ϊ������ѧ�ƣ�