题目内容
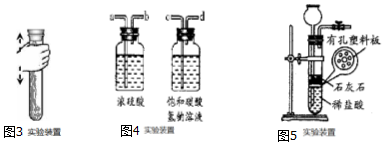
20.某兴趣小组围绕“酸和碱反应”的学习,进行了如图甲、乙所示的两个探究实验: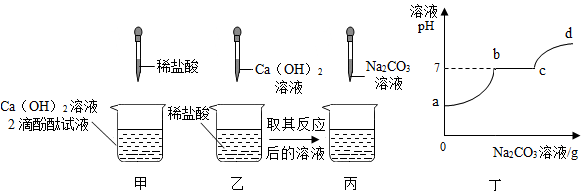
(1)实验甲在反应中加入酚酞溶液的目的是通过溶液颜色变化判断是否恰好完全反应.
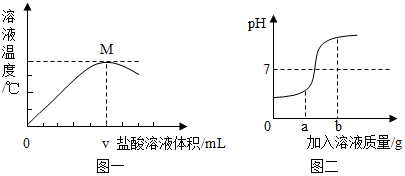
(2)取实验乙反应后的溶液逐滴滴加Na2CO3溶液,其pH变化如图丁所示.用试纸测定溶液pH的过程中,“用玻璃棒将溶液滴到试纸上”的后一步操作是与标准比色卡对比,图丁中d点溶液中所含的溶质是NaCl、Na2CO3(填化学式).
分析 氢氧化钙溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钙和水;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠.
解答 解:(1)氢氧化钙溶液中加入酚酞试液后溶液变红色,随着稀盐酸的不断滴加,溶液颜色变浅,当溶液恰好变成无色时,氢氧化钙和稀盐酸恰好完全反应,因此实验甲在反应中加入酚酞溶液的目的是通过溶液颜色变化判断是否恰好完全反应.
故填:通过溶液颜色变化判断是否恰好完全反应.
(2)用试纸测定溶液pH的过程中,“用玻璃棒将溶液滴到试纸上”的后一步操作是与标准比色卡对比;
a-b段是碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,b-c段是碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,c-d段是加入过量碳酸钠溶液,因此图丁中d点溶液中所含的溶质是反应生成的NaCl和过量的Na2CO3.
故填:与标准比色卡对比;NaCl、Na2CO3.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
4.使用pH试纸检验溶液的酸碱度时,正确的操作方法是( )
| A. | 使试纸一端浸入待测液中 | |
| B. | 用玻璃棒蘸取待测液滴在湿润的pH试纸上并跟标准比色卡对比 | |
| C. | 用玻璃棒蘸取待测液滴在pH试纸上并跟标准比色卡对比 | |
| D. | 以上方法都不对 |
9.镁被誉为“国防金属”,工业上通常用海水制取金属镁,有以下两个方案:
方案一:
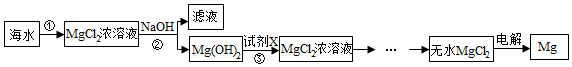
方案二:
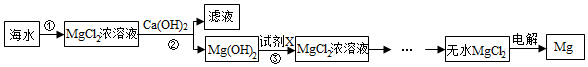
请回答下列问题:
(1)每吨试剂价格表:
工业生产为了获得更高的利润,根据上表分析,最好选择方案二(填“一”或“二”).
(2)步骤②中加入试剂充分反应后的操作是过滤;
(3)步骤③发生反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O;
(4)在MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑反应中化合价发生变化的元素有2种.
方案一:

方案二:

请回答下列问题:
(1)每吨试剂价格表:
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元/t) | 3200 | 1200 |
(2)步骤②中加入试剂充分反应后的操作是过滤;
(3)步骤③发生反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O;
(4)在MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑反应中化合价发生变化的元素有2种.
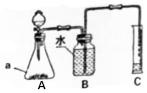 如图为实验室制取并收集一定体积气体(或测量生成气体体积)为分液漏斗图的实验装置图.
如图为实验室制取并收集一定体积气体(或测量生成气体体积)为分液漏斗图的实验装置图.

 实验室用一定质量的氯酸钾和二氧化锰制取氧气,回答下列问题.
实验室用一定质量的氯酸钾和二氧化锰制取氧气,回答下列问题.
