题目内容
3.某学生用量筒量取液体时,将量筒放平,倒入液体,面对刻度线,第一次俯视凹液面最低处,读数为19mL;倒出部分液体后,又平视凹液面最低处,读数为11mL.则该学生倒出的液体实际体积是( )| A. | 8mL | B. | 大于8mL | C. | 小于8mL | D. | 无法判断 |
分析 用量筒量取液体时,量筒要放平,读数时视线应与凹液面最低处相平;如果仰视液面,读数比实际偏小,若俯视液面,读数比实际偏大.根据量筒的读数与实际值的关系来判断该学生实际倒出液体的体积大小.
解答 解:用量筒量取液体时,量筒要放平,读数时视线应与凹液面最低处相平;如果仰视液面,读数比实际偏低,若俯视液面,读数比实际偏大.某同学读量筒中液体体积时,面向量筒刻度,俯视读数为19mL,其读数会比实际偏大,那么实际体积应小于19mL;倒出一部分液体后,视线与液体凹液面的最低处保持水平,读数为11mL,实际体积等于11mL,则该学生实际倾倒的液体体积小于8mL.
故选C.
点评 量筒的使用是中考热点之一,量筒操作错误时会出现“俯大仰小”,即俯视读数,数值比实际体积大,反之,则小.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.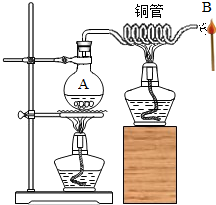 如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
 如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )
如图,加热A处瓶中水使之沸腾,水蒸气通过加热的铜管喷出,把火柴靠近铜管口一段时间后,从水蒸气中移开火柴,火柴被点燃了.下列说法正确的是( )| A. | B处水蒸气对火柴起引燃作用 | |
| B. | 火柴移离水蒸气才能燃烧是因为水蒸气具有助燃性 | |
| C. | 把螺旋状的铜管拉成直线型,实验效果更显著 | |
| D. | 该实验只证明了可燃物的燃烧需要足够的氧气 |
18.某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动.
提出问题:这瓶熟石灰粉末是否已经变质生成了CaCO3?
进行猜想:猜想一:熟石灰全部变成了CaCO3.
猜想二:熟石灰部分变成了CaCO3.
猜想一:熟石灰没有变质.
设计实验:该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容.
反思与应用:①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是试液变成红色.
②熟石灰变质是由于二氧化碳的缘故.在初中化学我们所学过的物质中还有氢氧化钠(举一例)等具有这样的性质,因此像熟石灰这类物质在实验室应密封保存.
提出问题:这瓶熟石灰粉末是否已经变质生成了CaCO3?
进行猜想:猜想一:熟石灰全部变成了CaCO3.
猜想二:熟石灰部分变成了CaCO3.
猜想一:熟石灰没有变质.
设计实验:该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞试液 ③取少量滤渣于试管中,加入盐酸 | ②试液没有变成红色. ③滤渣溶解,产生气泡. | 猜想一成立 |
②熟石灰变质是由于二氧化碳的缘故.在初中化学我们所学过的物质中还有氢氧化钠(举一例)等具有这样的性质,因此像熟石灰这类物质在实验室应密封保存.
15. 科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
①选择装置并检查气密性.
②称取0.1g的二氧化锰粉末加入容器中.
③量取20毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
④改变二氧化锰的质量,重复上述实验,记录数据如表.
(1)本实验探究的问题是二氧化锰的质量对过氧化氢分解快慢的影响.从表中数据分析得出的结论是其他条件相同时,二氧化锰的质量越大反应速率越快.
(2)写出实验室用过氧化氢溶液制取氧气反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)对于有气体生成的反应,要准确比较反应速率的快慢,除上述方法外,你还可以采用的方法是比较收集相同体积的气体所需时间的长短.
(4)为了完成本实验应选用的收集装置是③.(填序号)
(5)对于催化剂对化学反应速率的影响还有哪些因素,你可以大胆提出猜想,并设计实验进行验证.(要求仍以过氧化氢分解为例)
你的猜想:催化剂的种类不同影响过氧化氢分解的速率.
你的实验设计:(要有实验操作步骤、现象和结论)
步骤:在常温下,①分别称取0.1g的红砖粉末和二氧化锰加入到大试管内;②分别向大试管中加入20mL5%的过氧化氢溶液;③用排水法分别收集一瓶氧气并记录所需的时间
现象和结论:放入二氧化锰收集一瓶氧气所需的时间比放入红砖粉末的短,说明二氧化锰的催化效果比红砖粉末要好.
 科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.①选择装置并检查气密性.
②称取0.1g的二氧化锰粉末加入容器中.
③量取20毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
④改变二氧化锰的质量,重复上述实验,记录数据如表.
| 时间/秒 | 生成氧气的体积/毫升 | |||
| 0.1g MnO2 | 0.2g MnO2 | 0.3g MnO2 | 0.4g MnO2 | |
| 40 | 49 | 61 | 75 | 86 |
| 80 | 77 | 87 | 90 | 92 |
| 120 | 89 | 92 | 92 | 92 |
| 160 | 92 | 92 | 92 | 92 |
(2)写出实验室用过氧化氢溶液制取氧气反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)对于有气体生成的反应,要准确比较反应速率的快慢,除上述方法外,你还可以采用的方法是比较收集相同体积的气体所需时间的长短.
(4)为了完成本实验应选用的收集装置是③.(填序号)
(5)对于催化剂对化学反应速率的影响还有哪些因素,你可以大胆提出猜想,并设计实验进行验证.(要求仍以过氧化氢分解为例)
你的猜想:催化剂的种类不同影响过氧化氢分解的速率.
你的实验设计:(要有实验操作步骤、现象和结论)
步骤:在常温下,①分别称取0.1g的红砖粉末和二氧化锰加入到大试管内;②分别向大试管中加入20mL5%的过氧化氢溶液;③用排水法分别收集一瓶氧气并记录所需的时间
现象和结论:放入二氧化锰收集一瓶氧气所需的时间比放入红砖粉末的短,说明二氧化锰的催化效果比红砖粉末要好.
 小明同学发现他家菜园中的蔬菜生长迟缓发黄,他联系自己学过的生物知识估计到是缺氮肥了,于是就到农资商店去咨询购买,他发现商店里一种化肥的包装袋上的标签如图,请同学们帮计算:
小明同学发现他家菜园中的蔬菜生长迟缓发黄,他联系自己学过的生物知识估计到是缺氮肥了,于是就到农资商店去咨询购买,他发现商店里一种化肥的包装袋上的标签如图,请同学们帮计算:

