题目内容
11.熟练掌握化学用语是学好化学的重要工具.(1)3个镁离子3Mg2+;
(2)n个过氧化氢分子nH2O2;
(3)氯离子Cl-;
(4)氯化亚铁中铁元素的化合价为+2价$\stackrel{+2}{Fe}$Cl2.
(5)写出下列化学反应的化学式表达式:
①硫磺在氧气中燃烧:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2; ②利用双氧水制取氧气:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;;
③二氧化碳通入石灰水中:CO2+Ca(OH)2=CaCO3↓+H2O; ④氯酸钾与二氧化锰受热分解:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个镁离子可表示为:3Mg2+;
(2)分子的表示方法:正确书写物质的化学式,如五氧化二磷分子是多原子分子,可表示为:P2O5,表示多个该分子,就在其化学式前加上相应的数字,所以n个过氧化氢分子可表示为nH2O2;
(3)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故氯离子可表示为:Cl-;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氯化亚铁中铁元素的化合价为+2价,故可表示为:$\stackrel{+2}{Fe}$Cl2;
(5)①硫在氧气中燃烧生成二氧化硫,化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
②双氧水在二氧化锰的催化作用下分解生成水和氧气,故双氧水制取氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③二氧化碳能使石灰水中的氢氧化钙反应生成碳酸钙白色沉淀和水.化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
④氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
故答案为:(1)3Mg2+ (2)nH2O2 (3)Cl- (4)$\stackrel{+2}{Fe}$Cl2 (5)①S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;②2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③CO2+Ca(OH)2=CaCO3↓+H2O;④2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

| A. | 原子得到电子变成阴离子,所以一切微粒得到电子都会变成阴离子 | |
| B. | 单质是由一种元素组成,所以由一种元素组成的物质是单质 | |
| C. | N2、O2、CO2气体是由分子构成的,所以气体都是由分子构成的 | |
| D. | 分子、原子是不带电的粒子,但不带电的粒子不一定是分子、原子 |
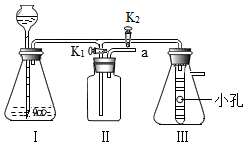 在CO2复习课上,小组合作激发了师生学习的热情:
在CO2复习课上,小组合作激发了师生学习的热情:(一)老师设计了如图所示的实验装置,既可用于制取CO2,又可用于探究CO2性质.
说明:
1、装置Ⅰ中盛放的药品是石灰石和稀盐酸.
2、装置Ⅲ中在小试管外壁贴有4片试纸:其中两端的两片用紫色石蕊溶液润湿,中间两片用紫色石蕊溶液浸过并晒干.
(1)实验时,打开K1,关闭K2,可用来制备CO2.Ⅰ中反应的化学式表达式为CaCO3+2HCl═CaCl2+H2O+CO2↑,检验Ⅱ中气体收集满的方法是将燃着的木条放至导管口a处,木条熄灭说明收集满.
(2)实验时,关闭K1,打开K2,可用于探究CO2的性质.实验时Ⅲ中出现的现象是干燥试纸无变化,湿润试纸由下至上依次变红,有关反应的化学式表达式为CO2+H2O═H2CO3,该实验说明CO2具有的性质是密度比空气大、能与水反应.
(二)同学们把一瓶CO2气体(排空气法收集,并已验满)倒扣在盛水的水槽中,有的小组没有观察到水压入瓶中,有的小组观察到少量水压入瓶中.针对课堂中出现的现象,化学小组的同学在课外进行了探究.
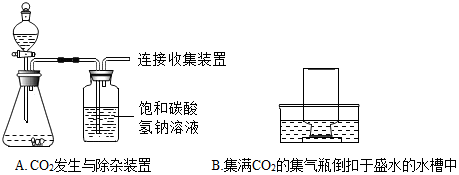
【提出问题】按教材的说法“1体积水大约能溶解1体积CO2”,水槽中的水足够把集气瓶中的CO2气体全部溶解,为什么集气瓶中的水面不上升或上升很少呢?
【作出猜想】
1、排空气法收集到的CO2气体可能不纯.
2、CO2溶于水需要时间较长.
3、…
【进行实验】小组同学分别用排空气法和排水法各收集2瓶CO2,重复图B实验,在不同时间测得压入的水量占集气瓶容积的百分数,数据见表1.
(已知:CO2在饱和碳酸氢钠溶液中溶解度很小)
表1 24小时内CO2溶解情况
| 气体样本 | 1 | 2 | 3 | 4 |
| 收集方法 | 向上排空气法 | 向上排空气法 | 排水法 | 排水法 |
| 2小时 | 13.7% | 15.0% | 15.3% | 15.1% |
| 24小时 | 35.7% | 56.3% | 94.2% | 93.6% |
课堂中同学们没有观察到预期实验现象的原因是时间短,排空气法收集的气体不纯.
【实验反思】
该实验引发了同学们对向上排空气法收集CO2的纯度及CO2收集方法的思考.
(1)向上排空气法收集CO2的纯度.
小组同学用容积为150mL 的集气瓶,装入部分水,留一定量的空气,用CO2排出这些水.用此法收集到占空气体积分数不同的CO2气体,再将燃着的木条伸入集气瓶中,观察是否熄灭.试验不同浓度的CO2使燃着的木条熄灭的情况,实验结果见表 2.
表2 占空气体积分数不同的CO2使燃着的木条熄灭情况
| 实验1 | 实验2 | 实验3 | 实验4 | |
| 集气瓶中预留水的体积 | 60mL | 45mL | 42mL | 39mL |
| CO2的体积分数 | 40% | 30% | X | 26% |
| 燃着的木条状况 | 灭 | 灭 | 灭 | 不灭 |
(2)排水法和向上排空气法收集气体所需时间对照
小组同学分4组用排水法和排空气法分别收集1瓶(集气瓶容积相同)CO2气体,记录所需时间,如表3所示.
表3 排水法和向上排空气法收集1瓶气体所需时间对照
| 1 | 2 | 3 | 4 | |
| 排水法 | 35“ | 43“ | 43“ | 43“ |
| 排空气法 | 1'57“ | 1'15“ | 1'4“ | 1'12“ |
②综合上述实验,请你对CO2的两种收集方法做出评价:排水法比排空气法收集的气体纯度高且收集时间短.
| A. | 8mL | B. | 大于8mL | C. | 小于8mL | D. | 无法判断 |
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有少量气泡产生,带火星木条不复燃 | 过氧化氢在常温下分解产生氧气,但是反应慢. ( 填“快”或“慢”) 反应的文字表达式为: 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气. | 二氧化锰可以作为过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气. | |
| 实验三 | 向盛有5mL5%的过氧化氢溶液的试管中加入二氧化锰, 伸入带火星的木条 | 有大量气泡产生,火星的木条迅速复燃 | 二氧化锰能加快过氧化氢分解产生氧气的速率. |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是验证不是水分解产生氧气而是过氧化氢分解产生氧气.
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面:在实验前后进行了两次对二氧化锰的称量,其目的是证明验证二氧化锰在化学反应前后质量不改变.
第二方面:倾倒掉“实验三”反应后的液体,向剩余的固体中重新加入过氧化氢溶液,又有大量气泡产生,由此说明验证二氧化锰在化学反应前后化学性质不改变.