题目内容
9.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下: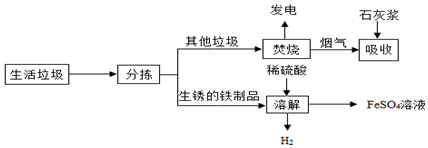
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化 ;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如表所示:
(仅在56.7℃或64℃温度下可同时析出两种晶体).
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
分析 (1)发电厂是利用垃圾焚烧产生的热能转变为电能;
(2)根据石灰浆是碱性分析;
(3)根据溶解过程中发生的化学反应来分析;
(4)根据氮气的化学性质来分析;
(5)根据图表中的信息可以知道当温度大于64℃时产生了FeSO4•4H2O,可以据此解答该题;
(6)根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁、二氧化硫和三氧化硫,可以据此写出该反应的化学方程式.
解答 解:(1)发电厂是利用垃圾焚烧产生的热能转变为电能;故填:热;
(2)石灰浆显碱性,能够吸收酸性气体,所以吸收步骤中,石灰浆的作用是除去烟气中含有的SO2、HCl;故填:Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);
(3)溶解步骤中,硫酸与铁反应,生成氢气,所以产生的H2的化学方程式为Fe+H2SO4═FeSO4+H2↑; 故填:Fe+H2SO4═FeSO4+H2↑;
(4)氮气的化学性质稳定,其中氮气的作用是作保护气,避免+2价的铁元素被空气中的氧气氧化;故填:保护气,避免+2价的铁元素被空气中的氧气氧化;
(5)根据图表中的信息可以知道当温度大于64℃时产生了FeSO4•4H2O,所以应该将温度控制在64℃以下;故填:不超过64℃;
(6)通过题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和三氧化硫,在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等,所以结合元素化合价的变化可以知道,铁元素的化合价由+2变成了+3价,所以反应中有二氧化硫生成,硫元素的化合价由+6降低到+4,所以根据质量守恒定律可以判断在该反应中还生成了三氧化硫,所以该反应的化学方程式为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.故填:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
点评 在解此类题时,应掌握化学方程式的书写、盐的化学性质等知识,并学会分析信息、提取信息,并根据所学知识结合所给信息进行解答.此题涉及的知识点较多,有一定的难度,需要同学们能够掌握全面的知识.

| A. | 水的电解实验说明水是由氢气和氧气组成的 | |
| B. | 保持水的化学性质的最小粒子是水分子 | |
| C. | 用活性炭可除去水中的色素和异味 | |
| D. | 水是一种常见的溶剂 |
| 选项 | 物 质 | 所含杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 加入过量碳酸钙粉末,过滤 |
| B | 二氧化碳 | 氧气 | 通过灼热的铜网 |
| C | CuO固体 | Fe3O4 | 用磁铁吸引 |
| D | NaCl溶液 | CaCl2 | 加入过量碳酸钠溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 提出问题 | B. | 设计实验 | C. | 进行实验 | D. | 分析与论证 |
【辨析俗称】“石灰干燥剂”中的石灰是指B (填字母)
A.消石灰 B.生石灰 C.石灰石
【猜想与假设】猜想一:石灰干燥剂没有变质;
猜想二:石灰干燥剂部分变质;
猜想三:石灰干燥剂完全变质.
【进行实验】兰兰分别取该石灰干燥剂进行如表实验,并记录.
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
| 实验一: 验证有无CaCO3 |  | 产生气泡 | 猜想一 不成立 |
| 实验二: 验证有无CaO |  | 无明显放热现象 | 猜想三 成立 |
【分析释疑】实验二的结论不准确,请用化学方程式解释烧杯壁明显发热的原因:CaO+H2O═Ca(OH)2
【更正结论】该石灰干燥剂部分变质,猜想二成立.
【反思与评价】石灰干燥剂表面的覆盖物,影响了正确结论的得出,兰兰由此联想到生活中有些物质表面的覆盖物,是起保护作用的,试举一例:铝制品表面的氧化膜.
【拓展延伸】从确定这包石灰干燥剂成分的角度,请你再提出一个具有探究价值的问题:该石灰干燥剂中是否含有氢氧化钙.
 铁是生产、生活中应用很广泛的一种金属,下列实验装置与铁的性质有关,请回答下列问题
铁是生产、生活中应用很广泛的一种金属,下列实验装置与铁的性质有关,请回答下列问题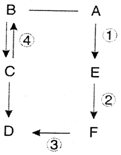 A、B、C、D、E、F都是初中化学中涉及的物质,已知A、B、C、D都是氧化物,且A是黑色固体,F是蓝色固体,相互间的转化关系如图(反应条件部分反应物、生成物略去),“-”表示连线两端的物质能发生反应,“→”表示一种物质能转化为另一种物质.回答:
A、B、C、D、E、F都是初中化学中涉及的物质,已知A、B、C、D都是氧化物,且A是黑色固体,F是蓝色固体,相互间的转化关系如图(反应条件部分反应物、生成物略去),“-”表示连线两端的物质能发生反应,“→”表示一种物质能转化为另一种物质.回答: