题目内容
17.化学的发展为人类文明作出了巨大贡献.请回答有关问题:(1)材料的发展推动社会的进步,材料技术和应用与化学科学的发展密切相关,下列材料属于合成材料的是B(填序号);
a.不锈钢 b.聚乙烯塑料 c.高强度陶瓷 d.钢筋混凝土
(2)化学科学为防治环境污染发挥重大作用.例如,用纳米级的某种氧化物做催化剂,使汽车尾气中的两种有毒气体CO与NO反应转化为两种无毒气体,其中一种是空气中含量最多的气体,这两种气体是CO2和N2;
(3)化学电源在生产、生活、科研中应用十分广泛.电池在使用时化学能转化为电能;
(4)化肥的发明和使用,大大提高了全球的粮食产量,其中“合成氨技术”、“尿素生产技术”等功不可没,在加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水,该反应的化学方程式是2NH3+CO2$\frac{\underline{\;加热\;}}{加压}$CO(NH2)2+H2O.
分析 (1)有机合成材料是指用有机高分子化合物制成的材料,可根据定义进行解答;
(2)根据题意以及质量守恒定律可知这两种气体是氮气和二氧化碳;
(3)根据化学电池的工作原理是将化学能转化为电能进行解答;
(4)根据加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水进行解答.
解答 解:(1)聚乙烯塑料属于有机合成材料,不锈钢属于金属材料,高强度陶瓷属于无机非金属材料,钢筋混凝土属于复合材料;
(2)用纳米级的某种氧化物做催化剂,使汽车尾气中的两种有毒气体CO与NO反应转化为两种无毒气体,其中一种是空气中含量最多的气体,这种气体就是氮气,另一种气体为二氧化碳;
(3)化学电池的工作原理是将化学能转化为电能;
(4)在加热、加压条件下,二氧化碳和氨气(NH3)反应生成尿素[CO(NH2)2]和水,该反应的化学方程式:2NH3+CO2$\frac{\underline{\;加热\;}}{加压}$CO(NH2)2+H2O.
故答案为:
(1)B;
(2)CO2;N2;
(3)化学;
(4)2NH3+CO2$\frac{\underline{\;加热\;}}{加压}$CO(NH2)2+H2O.
点评 了解化学研究的内容,才能利用化学知识服务于社会,造福于人类,有利于培养学生的学习兴趣,提高社会责任感.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂.下列有关丁酸乙酯的叙述正确的是( )
| A. | 丁酸乙酯是由碳、氢、氧三种原子构成的 | |
| B. | 丁酸乙酯中碳、氢、氧三种元素的质量比为3:6:1 | |
| C. | 丁酸乙酯中碳元素的质量分数为31% | |
| D. | 一个丁酸乙酯分子中含有20个原子 |
8.下列有关物质的用途的说法中正确的是( )
| A. | 氮气的化学性质不活泼,因而可用作保护气 | |
| B. | 氢氧化钠可用于治疗胃酸过多 | |
| C. | 活性炭具有吸附性,因此可用活性炭将硬水软化 | |
| D. | 氧气的化学性质比较活泼,因此液态氧常用作燃料 |
5.现有失去标签的两瓶无色固体:烧碱固体和纯碱固体.某兴趣小组设计用化学方法和物理方法区分它们.请回答有关问题:
(1)化学方法按表中方法一填写.所选试剂须属不同物质类别.
(2)物理方法(简要叙述操作方法和判断方法)取样分别溶于水,温度明显升高的是烧碱,温度没有明显改变的是纯碱.
(1)化学方法按表中方法一填写.所选试剂须属不同物质类别.
| 物质类别 | 所选试剂 | 判断方法 |
| 酸 | 盐酸 | 取样分别与盐酸反应,有气体生成的是纯碱,没气体的是烧碱. |
| 碱 | ||
| 盐 |
12.蔬菜、水果可以调节新陈代谢、维持身体健康,主要原因是蔬菜、水果中富含人体需要量很少、作用却非常重要的( )
| A. | 蛋白质 | B. | 糖类 | C. | 维生素 | D. | 油脂 |
2.下列现象与名词不相对应的是( )
| 选项 | 现象 | 名词 |
| A | 氢氧化钠固体露置在空气中,表面变潮湿 | 潮解 |
| B | 把饱和硫酸铵溶液加入蛋白质溶液,有固体析出 | 盐析 |
| C | 打开装有浓盐酸的试剂瓶瓶塞,瓶口出现白雾 | 挥发 |
| D | 用洗洁精洗去餐具上的油污 | 溶解 |
| A. | A | B. | B | C. | C | D. | D |
9.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
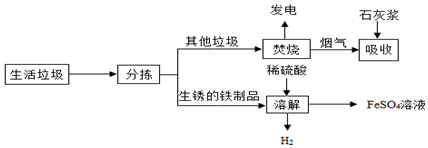
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化 ;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如表所示:
(仅在56.7℃或64℃温度下可同时析出两种晶体).
若需从硫酸亚铁溶液中结晶出FeSO4•4H2O,应控制的结晶温度(t)的范围为不超过64℃;
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.

资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化 ;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如表所示:
(仅在56.7℃或64℃温度下可同时析出两种晶体).
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
7.人体健康离不开化学,下列叙述错误的是( )
| A. | 铁、钴、铜、锌、钼是人体中的微量元素 | |
| B. | 蔗糖能在酶的催化作用下经缓慢氧化变成二氧化碳和水,同时放出热量 | |
| C. | 为了增加人体所需的营养成分,可在食品中添加适量的食品添加剂 | |
| D. | 不能用PVC的塑料袋来装食品 |