题目内容
19.化学知识与社会生产、日常生活密切相关,请用所学知识回答下列问题:(1)铁锅是人类最理想的炊具.使用铁锅有利于人体健康,主要是因为能增加人体或食物中的铁元素.
(2)铁是应用最广泛的金属.铁制品很容易生锈,其生锈的条件是与氧气、水同时接触,盐酸可用于除铁锈,写出盐酸除铁锈的化学方程式Fe2O3+6HCl=2FeCl3+3H2O.
(3)注意饮水安全,保证人体健康.在天然水净化的过程中,人们常用活性炭去除水的异味和色素,这是利用了活性炭的吸附性.此外还需要加入二氧化氯(ClO2)进行杀菌和消毒,在二氧化氯(ClO2)中氯元素的化合价为+4.
分析 (1)根据已有的铁元素与人体健康的知识解答;
(2)根据氧化铁能与盐酸反应生成氯化铁和水解答;
(3)根据活性炭具有吸附性,根据化合价规则解答,根据食物中的营养素解答.
解答 解:(1)使用铁锅有利于人体健康,是因为能增加人体或食物中的铁元素,故填:能增加人体或食物中的铁元素;
(2)铁是应用最广泛的金属.铁制品很容易生锈,其生锈的条件是与氧气、水同时接触,氧化铁能与盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
(3)活性炭具有吸附性,能吸附色素和异味,在二氧化氯中,氧元素的化合价为-2,设氯元素的化合价为x,则有x+(-2)×2=0,解得x=+4,故填:吸附,+4;
答案:
(1)能增加人体或食物中的铁元素;
(2)与氧气、水同时接触;Fe2O3+6HCl=2FeCl3+3H2O;
(3)吸附;+4.
点评 本题考查的是化学与生活的知识,完成此题,可以依据已有的知识进行.要加强对基础知识的掌握,以便灵活应用.

练习册系列答案
相关题目
9.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
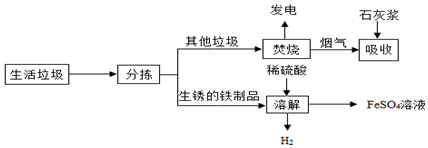
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化 ;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如表所示:
(仅在56.7℃或64℃温度下可同时析出两种晶体).
若需从硫酸亚铁溶液中结晶出FeSO4•4H2O,应控制的结晶温度(t)的范围为不超过64℃;
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.

资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:(1)焚烧垃圾发电厂是将垃圾焚烧后获得的热能,最终转化为电能;
(2)在上述流程的“吸收”步骤中,石灰浆的作用是Ca(OH)2+SO2=CaSO3+H2O(或Ca(OH)2+2HCl=CaCl2+H2O);(用其中任1个反应的化学方程式表示)
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,其中有单质生成的化学方程式是Fe+H2SO4═FeSO4+H2↑;
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是保护气,避免+2价的铁元素被空气中的氧气氧化 ;
(5)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4•7H2O、FeSO4•4H2O和FeSO4•H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如表所示:
(仅在56.7℃或64℃温度下可同时析出两种晶体).
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(6)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它二种硫的氧化物,试写出该反应的化学方程式2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
7.人体健康离不开化学,下列叙述错误的是( )
| A. | 铁、钴、铜、锌、钼是人体中的微量元素 | |
| B. | 蔗糖能在酶的催化作用下经缓慢氧化变成二氧化碳和水,同时放出热量 | |
| C. | 为了增加人体所需的营养成分,可在食品中添加适量的食品添加剂 | |
| D. | 不能用PVC的塑料袋来装食品 |
14.下图所示实验中不能达到实验目的是( )
| A. |  区分软硬水 | B. | 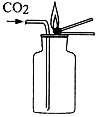 检验CO2是否收集满 | ||
| C. | 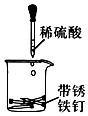 除去铁钉上的铁锈 | D. |  验证NaCl溶液中是否混有盐酸 |
11.下列化学用语与所表达的意义对应正确的是( )
| A. | 2N2--2个氮原子 | B. | 2H--2个氢元素 | ||
| C. | CO3-2--碳酸根离子 | D. | 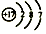 --氯原子的结构示意图 --氯原子的结构示意图 |
9.下列是探究灭火原理的四个实验,其中说法不正确的是( )
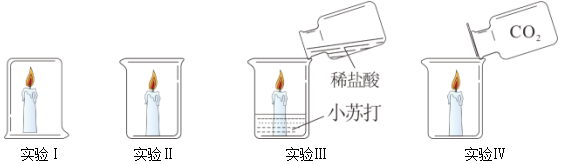

| A. | 实验Ⅰ中蜡烛熄灭、实验Ⅱ中蜡烛不熄灭,说明隔绝空气可以灭火 | |
| B. | 通过上述实验能得出,灭火原理包括隔绝氧气、降低温度、隔离可燃物 | |
| C. | 实验Ⅲ中蜡烛熄灭,因为稀盐酸与小苏打反应生成二氧化碳隔绝了空气 | |
| D. | 实验Ⅳ中蜡烛熄灭,说明二氧化碳的密度比空气大且不能燃烧不支持燃烧 |
 兴趣小组的同学用如图所示装置做了相关实验.
兴趣小组的同学用如图所示装置做了相关实验.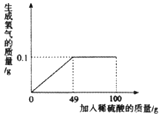 实验室存在的一瓶稀硫酸标签被腐蚀,小明同学想通过实验测定该稀硫酸的溶质质量分数.取一定量的锌粒加入稀硫酸100g,所加稀硫酸与生成氢气的质量关系如图所示:请完成下列分析及计算:
实验室存在的一瓶稀硫酸标签被腐蚀,小明同学想通过实验测定该稀硫酸的溶质质量分数.取一定量的锌粒加入稀硫酸100g,所加稀硫酸与生成氢气的质量关系如图所示:请完成下列分析及计算: