题目内容
在金属活动性顺序里,钠位于铜之前.某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜.该小组同学对此现象进行了如下探究:
[查阅资料]
钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应.
[分析与讨论]
(1)在实验室中通常将钠保存在煤油里,煤油的作用是 .
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低.对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为 同学的猜想不合理,请从化合价的角度解释原因: .
[进行实验]该小组同学通过实验验证钠与水反应的产物,装置如图:
[解释与结论]
将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写): , .
[查阅资料]

钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应.
[分析与讨论]
(1)在实验室中通常将钠保存在煤油里,煤油的作用是
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低.对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为
[进行实验]该小组同学通过实验验证钠与水反应的产物,装置如图:
[解释与结论]
将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写):
| 实验操作 | 实验现象及分析 | |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞. | 实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中. 钠的物理性质有: |
| ② | 打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b. | 发生反应的化学方程式为: |
| ③ | 打开止水夹c. | 实验现象为:D中液体 |
| ④ | 打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口. | 实验现象为:气体燃烧,产生 |
| ⑤ | 在火焰上方罩一个干冷的烧杯. | 实验现象为:烧杯内壁出现 |
考点:实验探究物质的性质或变化规律
专题:科学探究
分析:[分析与讨论](1)根据钠与氧气和水反应进行解答;
(2)根据若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低进行解答;
[解释与结论]根据钠和水反应生成氢氧化钠和氢气以及氢氧化钠和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠进行解答;
①根据物质的物理性质不需要通过化学变化变现进行解答;
②根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水进行解答;
③根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水使得C内压强变小进行解答;
④根据氢气燃烧的现象进行解答;
⑤根据氢气燃烧生成水进行解答.
(2)根据若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低进行解答;
[解释与结论]根据钠和水反应生成氢氧化钠和氢气以及氢氧化钠和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠进行解答;
①根据物质的物理性质不需要通过化学变化变现进行解答;
②根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水进行解答;
③根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水使得C内压强变小进行解答;
④根据氢气燃烧的现象进行解答;
⑤根据氢气燃烧生成水进行解答.
解答:解:[分析与讨论](1)钠与氧气和水反应,所以在实验室中通常将钠保存在煤油里,煤油的作用是将钠与氧气和水隔绝;
(2)根据在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低.若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低,所以乙同学的猜想不合理;
[解释与结论]钠和水反应生成氢氧化钠和氢气,发生反应的化学方程式2Na+2H2O=2NaOH+H2↑;氢氧化钠和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,发生反应的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
①物质的物理性质不需要通过化学变化变现,钠的物理性质有:银白色固体,熔点低,密度比水小、比煤油大等;
②二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,发生反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
③二氧化碳和氢氧化钠溶液反应生成碳酸钠和水使得C内压强变小,实验现象为:D中液体倒吸入C中,C中产生气泡;
④氢气燃烧的现象:气体燃烧,产生淡蓝色火焰;
⑤氢气燃烧生成水,所以在火焰上方罩一个干冷的烧杯,烧杯内壁出现无色液滴.
故答案为:【分析与讨论】(1)将钠与氧气和水隔绝;
(2)乙;若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低;
【解释与结论】2Na+2H2O=2NaOH+H2↑;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
【进行实验】
(2)根据在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低.若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低,所以乙同学的猜想不合理;
[解释与结论]钠和水反应生成氢氧化钠和氢气,发生反应的化学方程式2Na+2H2O=2NaOH+H2↑;氢氧化钠和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,发生反应的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
①物质的物理性质不需要通过化学变化变现,钠的物理性质有:银白色固体,熔点低,密度比水小、比煤油大等;
②二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,发生反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
③二氧化碳和氢氧化钠溶液反应生成碳酸钠和水使得C内压强变小,实验现象为:D中液体倒吸入C中,C中产生气泡;
④氢气燃烧的现象:气体燃烧,产生淡蓝色火焰;
⑤氢气燃烧生成水,所以在火焰上方罩一个干冷的烧杯,烧杯内壁出现无色液滴.
故答案为:【分析与讨论】(1)将钠与氧气和水隔绝;
(2)乙;若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到+1价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低;
【解释与结论】2Na+2H2O=2NaOH+H2↑;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
【进行实验】
| 实验现象及分析 | |
| ① | 银白色固体,熔点低 |
| ② | CO2+2NaOH=Na2CO3+H2O |
| ③ | 倒吸入C中 |
| ④ | 淡蓝 |
| ⑤ | 无色液滴 |
点评:该题要求学生再掌握金属的活动性强弱和一些常用物质的颜色的同时,还要求学生具有综合分析问题的能力以及具有类比推断的能力.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
氧化银钮扣电池常用于手表和计算机,电池内的总反应可以表示为:Zn+Ag2O═ZnO+2Ag.关于该反应的下列说法正确的是( )
| A、该反应属于化合反应 |
| B、该反应属于复分解反应 |
| C、该反应属于置换反应 |
| D、该反应中银元素的化合价升高 |
同一种元素往往能形成不同种单质,这些单质互称为同素异形体.下列各组物质互称为“同素异形体”的是( )
| A、红磷和白磷 |
| B、CO和CO2 |
| C、液氧和氧气 |
| D、石灰石和大理石 |
绿色能源不会产生或残留对环境造成污染的物质,下列能源中不能称为绿色能源的( )
| A、煤 | B、氢能 | C、风能 | D、太阳能 |
下列物质由原子构成的是( )
| A、氯化钠 | B、蒸馏水 | C、氮气 | D、铁 |
在①HNO3、HCl、KNO3、H2SO4②SO3、H2O、P2O5、Na2O③O3、H2、CO、N2三组物质中,各有一种物质在分类上与组内的其他物质不同,这三种物质分别是( )
| A、KNO3、Na2O、CO |
| B、HNO3、Na2O、CO |
| C、H2SO4、P2O5、H2 |
| D、KNO3、SO3、N2 |
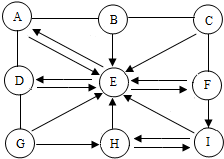 如图中的A-I所表示物质均为初中化学常见的纯净物.其中A、D是非金属单质;B、E、H 是氧化物;B中氧元素质量分数为20%且为黑色粉末;G是天然气的主要成分;C、F、I是三种不同类别的无机化合物;F常用于改良酸性土壤.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系.(部分反应物或生成物已略去)
如图中的A-I所表示物质均为初中化学常见的纯净物.其中A、D是非金属单质;B、E、H 是氧化物;B中氧元素质量分数为20%且为黑色粉末;G是天然气的主要成分;C、F、I是三种不同类别的无机化合物;F常用于改良酸性土壤.图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系.(部分反应物或生成物已略去) 我们学过有六种途径制取氧气,如图所示:
我们学过有六种途径制取氧气,如图所示: