题目内容
18.下列关于氧气(O2)和臭氧(O3)的说法正确的是( )| A. | 氧气是纯净物,臭氧是混合物 | B. | 氧气是单质,臭氧是化合物 | ||
| C. | 氧气由氧元素组成,而臭氧不是 | D. | 氧气和臭氧都是单质 |
分析 氧气和臭氧属于氧元素组成的单质,它们是不同的物质.
解答 解:A、氧气和臭氧都是纯净物,错误;
B、氧气和臭氧都是单质,错误;
C、氧气和臭氧属于氧元素组成的单质,错误;
D、氧气和臭氧都是单质,正确.
故选D.
点评 本题的难度不大,了解氧气(O2)和臭氧(O3)的组成特点是解答本题的基础.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
8.下列说法正确的是( )
①工业上采用分离液态空气的方法制备氧气和氮气
②氢气等可燃性气体在点燃前要检验气体的纯度
③一般情况下合金的熔点和硬度都比组成合金的纯金属高
④氢氧化钠固体潮解、变质与水蒸气和二氧化碳有关
⑤二氧化碳、二氧化硫、二氧化氮和一氧化碳都是大气污染物.
①工业上采用分离液态空气的方法制备氧气和氮气
②氢气等可燃性气体在点燃前要检验气体的纯度
③一般情况下合金的熔点和硬度都比组成合金的纯金属高
④氢氧化钠固体潮解、变质与水蒸气和二氧化碳有关
⑤二氧化碳、二氧化硫、二氧化氮和一氧化碳都是大气污染物.
| A. | ②③④ | B. | ①②④ | C. | ①③⑤ | D. | ③④⑤ |
6.La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3难溶于水,而LaCl3、La(NO3)3都易溶于水.下列各组物质中,不能直接反应生成LaCl3的是( )
| A. | La+HCl | B. | La2O3+HCl | C. | NaCl+La(NO3)3 | D. | La(OH)3+HCl |
13.下列实验操作正确的是( )
| A. | 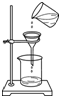 | B. | 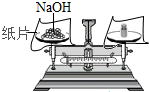 | C. | 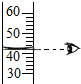 | D. |  |
10.科学家在一定条件下将一氧化碳与氢气合成甲醇(CH3OH),下列说法正确的是( )
| A. | 甲醇为无机物 | |
| B. | 甲醇由碳原子、氧原子、氢原子构成 | |
| C. | 甲醇中碳元素与氢元素的质量比为1:4 | |
| D. | 该合成过程CO和H2的质量比为7:1 |
8.已知某金属粉末中可能含有铁、铝、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究.
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由铁和铜组成.
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,铁和铜与氢氧化钠溶液均不发生反应.
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水.
【进行实验】
【反思与评价】实验中发生反应的化学方程式为Fe+2HCl=FeCl2+H2↑.
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由铁和铜组成.
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,铁和铜与氢氧化钠溶液均不发生反应.
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水.
【进行实验】
| 实验目的 | 实验操作 | 实验现象 | 实验结论 |
| 证明粉末中是否含有铝粉 | 取一个小烧杯,加入适量的粉末,再向其中加入足量的氢氧化钠溶液 | 无明显变化 | 猜想四成立; |
| 证明粉末中是否含有铁粉 | 过滤,将得到的固体洗涤后放入小烧杯,再向其中加入足量的稀盐酸 | 有气泡产生,固体未完全溶解 |