题目内容
17.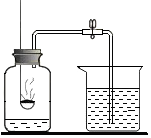 实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:(1)集气瓶内水面上升约$\frac{1}{5}$体积,由此你得到的结论是:氧气约占空气总体积的五分之一.
(2)实验中的红磷需要稍微过量,目的是完全消耗瓶内氧气.请写出红磷燃烧这一反应的(文字或符号)表达式:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)通过这个实验,我们还可以认识氮气的一些性质.请将你的分析结果填在如表
的横线上.
| 实 验 现 象 | 分 析 结 果(即氮气的性质) |
| ①燃烧着的红磷慢慢熄灭了 | 氮气不支持燃烧 |
| ③集气瓶内的水面上升一定高度后不再上升 | 氮气不易溶于水 |
分析 (1)根据进入集气瓶中的水的量,可以判断氧气的体积分数;
(2)根据实验结果的严密性和反应原理来分析解答;
(3)根据实验现象来分析氮气的性质.
解答 解:(1)实验结束后,打开止水夹时,进入集气瓶中的水约占集气瓶容积的五分之一.进入集气瓶的水的体积即为被消耗的氧气的体积,由此可得出的结论是氧气约占空气总体积的五分之一.故填:氧气约占空气总体积的五分之一.
(2)实验中红磷需要过量,是为了将集气瓶中的氧气完全耗尽,磷与氧气在点燃的条件下反应生成五氧化二磷;故填:完全消耗瓶内氧气;磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(3)①燃烧着的红磷慢慢熄灭了,此时红磷仍有剩余,这说明了氮气不支持燃烧;故填:氮气不支持燃烧;
②集气瓶内的水面上升一定高度后不再上升,这一现象说明氮气是不易溶于水的,故填:氮气不易溶于水.
点评 本题以空气中氧气的含量为载体,考查了相关化学方程式的书写、所测氧气含量偏低的原因、氮气的性质等,考查学生科学探究和逻辑思维的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.除去下列物质中的少量杂质.所选用的试剂正确的是
| 选项 | 物质 | 杂质 | 试剂 |
| A | 木炭粉 | MnO2 | 适量水 |
| B | Mg粉 | Cu粉 | 足量稀硫酸 |
| C | FeCl3溶液 | CuCl2 | 过量铁粉 |
| D | NaCl | MgCl2 | 足量饱和食盐水 |
| A. | A | B. | B | C. | C | D. | D |
5.氯原子得到一个电子变成离子后,发生改变的是( )
| A. | 元素种类 | B. | 核外电子数 | C. | 电子层数 | D. | 相对原子质量 |
9.某校科学探究小组同学把一块捡来的石灰石做纯度分析,进行了如下实验:
他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:
取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(反应生成的氯化钙能溶于水,杂质不溶于水,也不与盐酸反应).
请计算:
(1)上表中的m=3
(2)样品中的碳酸钙的质量分数是多少?
(3)整个实验过程中共生成二氧化碳的质量为多少?
他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:
取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(反应生成的氯化钙能溶于水,杂质不溶于水,也不与盐酸反应).
| 序 号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体质量(g) | 5.5 | m | 1.6 | 1.6 |
(1)上表中的m=3
(2)样品中的碳酸钙的质量分数是多少?
(3)整个实验过程中共生成二氧化碳的质量为多少?
 当你参加“以水为题”的课外小组活动时,请根据以下活动内容,回答问题.
当你参加“以水为题”的课外小组活动时,请根据以下活动内容,回答问题.


