题目内容
6. 当你参加“以水为题”的课外小组活动时,请根据以下活动内容,回答问题.
当你参加“以水为题”的课外小组活动时,请根据以下活动内容,回答问题.(1)从姑溪河取水样后,制成两个如图所示的简易净水器,对河水进行初步净化.请问,简易净水器I中,用到了小卵石、石英砂和膨松棉.其中小卵石的作用为(填代号)B,活性炭的作用为(填代号)C;
A.沉淀 B.过滤 C.吸附 D.使硬水软化 E.使浑浊的水变成纯净物水
(2)硬水给生活和生产会带来很多麻烦,可用肥皂水来区分硬水和软水,生活中常用用来降低水的硬度的方法是煮沸.
(3)使用简易净水器Ⅱ处理河水时,若过滤后滤液仍然浑浊,造成该现象的原因是:滤纸破损 (写一点).
分析 (1)净水器中小卵石、石英砂和膨松棉的作用是过滤,活性炭可吸附色素、异味等;
(2)据过滤的注意事项分析解答;
(3)硬水是指水中含有较多的可溶性钙、镁的化合物,软水是指含的少或没有,硬水和软水的区别就是加入肥皂水,泡沫较多的是软水,较少的是硬水;
(4)可以根据过滤注意事项来解答.
解答 解:(1)小卵石的作用为过滤,活性炭的作用为吸附.故填:B; C.
(2)用肥皂在实验室的自来水中洗衣时,起浮渣,说明该自来水是含较多可溶的钙、镁化合物的水,属于硬水..生活中常用加热煮沸降低水的硬度;
(4)如果过滤后滤液仍然浑浊,造成该现象的原因是滤纸破损或液面高于滤纸的边缘,故填:滤纸破损.
答案:(1)B; C; (2)肥皂水;煮沸;(3)滤纸破损(答案合理均可)
点评 解答本题要充分理解净化水的方法,只有这样才能对问题做出正确的判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16. 化学学习小组的同学们在探究氢氧化钠的性质时,将CO2通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将CO2通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
探究一:CO2是否与氢氧化钠发生了化学反应?
为了证明CO2与氢氧化钠的确发生了化学反应,你选择的物质是c、d、e(填写字母).请任意选择一个能证明CO2与氢氧化钠发生反应的化学方程式Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
a.无色酚酞溶液 b.硝酸钠溶液 c.硫酸
d.硝酸钡溶液 e.Ba(OH)2溶液
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】
佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH.
写出CO2与氢氧化钠反应的化学方程式2NaOH+CO2=Na2CO3+H2O;
【实验验证】
佳佳同学取实验后的溶液滴加酚酞溶液,观察到无色酚酞溶液变红色,则证明自己的猜想正确.该实验设计是否合理不合理,其理由是含有碳酸钠的溶液和含有氢氧化钠的溶液均显碱性,都能使无色酚酞溶液变红;
贝贝为了验证自己的猜想,进行了如下实验,请你补充完整.
【实验反思】
①要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
②同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否反生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴加边测定混合溶液的pH.请你分析上述方案中,只强调pH变小为什么要“当测定pH小于或等于7”才可证明发生了反应,其原因是稀硫酸中的水会稀释氢氧化钠,使ph值变小.当ph值小于等于7时,说明氢氧化钠消耗完毕,则说明氢氧化钠和稀硫酸反应.
 化学学习小组的同学们在探究氢氧化钠的性质时,将CO2通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将CO2通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.探究一:CO2是否与氢氧化钠发生了化学反应?
为了证明CO2与氢氧化钠的确发生了化学反应,你选择的物质是c、d、e(填写字母).请任意选择一个能证明CO2与氢氧化钠发生反应的化学方程式Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
a.无色酚酞溶液 b.硝酸钠溶液 c.硫酸
d.硝酸钡溶液 e.Ba(OH)2溶液
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】
佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH.
写出CO2与氢氧化钠反应的化学方程式2NaOH+CO2=Na2CO3+H2O;
【实验验证】
佳佳同学取实验后的溶液滴加酚酞溶液,观察到无色酚酞溶液变红色,则证明自己的猜想正确.该实验设计是否合理不合理,其理由是含有碳酸钠的溶液和含有氢氧化钠的溶液均显碱性,都能使无色酚酞溶液变红;
贝贝为了验证自己的猜想,进行了如下实验,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
①取一定量大试管中的溶液于试管中,加入足量CaCl2溶液,过滤 ②向滤液滴加适量无色酚酞试液 | ①产生白色沉淀 ②溶液变红 | 贝贝的猜想成立 |
①要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
②同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否反生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴加边测定混合溶液的pH.请你分析上述方案中,只强调pH变小为什么要“当测定pH小于或等于7”才可证明发生了反应,其原因是稀硫酸中的水会稀释氢氧化钠,使ph值变小.当ph值小于等于7时,说明氢氧化钠消耗完毕,则说明氢氧化钠和稀硫酸反应.
17.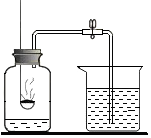 实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
(1)集气瓶内水面上升约$\frac{1}{5}$体积,由此你得到的结论是:氧气约占空气总体积的五分之一.
(2)实验中的红磷需要稍微过量,目的是完全消耗瓶内氧气.请写出红磷燃烧这一反应的(文字或符号)表达式:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)通过这个实验,我们还可以认识氮气的一些性质.请将你的分析结果填在如表
的横线上.
 实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:
实验室可用如图所示装置来测定空气中氧气的含量.实验时可观察到:当红磷在集气瓶中燃烧停止后,集气瓶内水面上升大约$\frac{1}{5}$体积.请你回答:(1)集气瓶内水面上升约$\frac{1}{5}$体积,由此你得到的结论是:氧气约占空气总体积的五分之一.
(2)实验中的红磷需要稍微过量,目的是完全消耗瓶内氧气.请写出红磷燃烧这一反应的(文字或符号)表达式:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)通过这个实验,我们还可以认识氮气的一些性质.请将你的分析结果填在如表
的横线上.
| 实 验 现 象 | 分 析 结 果(即氮气的性质) |
| ①燃烧着的红磷慢慢熄灭了 | 氮气不支持燃烧 |
| ③集气瓶内的水面上升一定高度后不再上升 | 氮气不易溶于水 |
1.如图是水分子在一定条件下分解的示意图,下列说法不正确的是( )

| A. | 一个水分子由两个氢原子和一个氧原子构成 | |
| B. | 水分解后生成氢气和氧气的分子数比为2:1 | |
| C. | 水分解过程中,原子的数目不变 | |
| D. | 水分解过程中,分子的种类不变 |
18.下列四种粒子的结构示意图中,说法正确的是( ) 

| A. | 它们表示四种不同的元素 | |
| B. | ②③④表示的元素都是非金属元素 | |
| C. | ③表示的元素在化合物中通常显+1价 | |
| D. | ①③表示的是阳离子 |
15.下列物质中属于纯净物的是( )
| A. | 白醋 | B. | 洁净的空气 | C. | 苏打水 | D. | 冰水混合物 |
16.除去CO2中混有的少量CO,可使混合气体通过( )
| A. | 点燃 | B. | 澄清石灰水 | ||
| C. | 灼热的炭层 | D. | 灼热的氧化铜粉末 |