题目内容
6.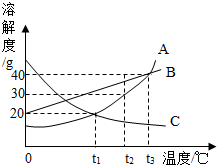 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.(1)t3℃时,A、B、C三种物质的溶解度大小关系是A=B>C.
(2)在保持溶液质量分数不变的前提下,使接近饱和的A物质溶液变成饱和溶液,可以采用的方法是降温.
(3)t1℃时,将一定量C的饱和溶液升温至t2℃,溶液的质量将减少
(填“增加”、“减少”或“不变”).
(4)A、B、C三种物质各30g分别溶于100g水中,当温度控制在t1℃<t<t2℃时,所得溶液中溶质质量分数最大的是B物质.
分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降低温度,并结合A的溶解度随温度变化趋势分析解答;
(3)据C的溶解度随温度变化情况分析升温对溶质的质量的影响;
(4)结合该温度范围内物质的溶解度,及溶液中溶质的质量分数计算式分析解答
解答 解:(1)据溶解度曲线可知:t3℃时,A、B、C三种物质的溶解度大小关系为 A=B>C;
(2)A的溶解度随温度的升高而增大,因此使一定量接近饱和的A物质溶液变为饱和溶液,可采用降温、加入A、蒸发溶剂的方法;在保持溶液质量分数不变的前提下,只能选择降温;
(3)C的溶解度随温度的升高而减小,所以t1℃时,将一定量C的饱和溶液升温至t2℃,将会析出晶体,溶液的质量将减小;
(4)观察图示可知:t2℃时A的溶解度是30g,当温度控制在大于t1℃小于t2℃时,A的溶解度最大是30g,而B的溶解度始终大于30g,C的溶解度始终小于30g,所以在此温度范围内,所得溶液中溶质质量分数最大的是B;
故答案为:(1)A=B>C (2)降温 (3)减少 (4)B
点评 本题主要考查了溶解度曲线的意义及不饱和溶液和饱和溶液的相互转化等知识,较好考查了学生应用知识解决问题的能力.

练习册系列答案
相关题目
16.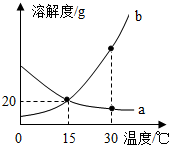 a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
 a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | a、b的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将30℃时a的饱和溶液(溶液底部无晶体)降温至15℃,溶质的质量分数不变 | |
| D. | 分别向100g水中加入20ga和b,升温至30℃,所得溶液均为饱和溶液 |
14.下列关于100g 5%NaOH溶液的配制和应用说法正确的是( )
| A. | 配制时,用50mL量筒分两次共量取95.0mL水 | |
| B. | 称量时,应将NaOH固体放入小烧杯或表面皿中称量 | |
| C. | 将配好的溶液倒入试剂瓶内,并贴上标签,标签上应写上“100g NaOH溶液” | |
| D. | 50g 20%NaOH溶液中加入100mL水稀释可得到5%Na0H溶液 |
1.下列说法不正确的是( )
| A. | 氮气用作保护气是利用了它的物理性质 | |
| B. | 氧气充足的燃烧可节约燃料 | |
| C. | 点燃氢气前一定要验纯 | |
| D. | 熟石灰可改良酸性土壤 |
15.我省阜阳盛产一种调味品生姜,生姜中含有姜辣素(C17H25O4)而有辛辣味,下列关于姜辣素的说法错误的是( )
| A. | C、H、O元素质量之比为17:26:4 | B. | 闻到辛辣味说明分子在不断运动 | ||
| C. | 属于有机化合物 | D. | 一个姜辣素分子中含有四个氧原子 |
16.下列生活用品中,属于纯净物的是( )
| A. | 加碘食盐 | B. | 食醋 | C. | 不锈钢钉 | D. | 蒸馏水 |

 代表氢原子,
代表氢原子, 代表氧原子)
代表氧原子)