题目内容
16.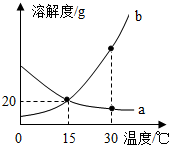 a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | a、b的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将30℃时a的饱和溶液(溶液底部无晶体)降温至15℃,溶质的质量分数不变 | |
| D. | 分别向100g水中加入20ga和b,升温至30℃,所得溶液均为饱和溶液 |
分析 A、根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小;
B、饱和溶液和不饱和溶液之间可以相互转化;
C、溶液中溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
D、根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和.
解答 解:A、a、b的溶解度在15℃时都是20g,其它温度时都不是20g,该选项说法不正确;
B、加水可使b的饱和溶液变为不饱和溶液,由于b的溶解度随着温度的升高而增大,因此b的饱和溶液降温时仍然是饱和溶液,该选项说法不正确;
C、30℃时,将a溶液降温至15℃,a的溶解度增大,没有析出晶体,因此溶质的质量分数一定不变,该选项说法正确;
D、分别向100g水中加入a和b的混合物20g,如果a的质量很小,升温至30℃,所得a溶液可能是不饱和溶液,如果a的质量较大,所得a溶液可能是饱和溶液,该选项说法不正确.
故选:C
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列关于相应微粒的描述中,正确的是( )
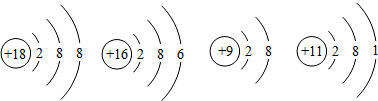
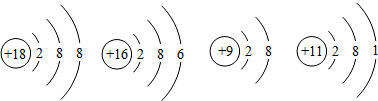
| A. | 化学性质活泼 | B. | 易形成阳离子 | C. | 带负电荷 | D. | 易得电子 |
11.下列反应中属于氧化反应,但是不属于化合反应的是( )
| A. | 铝+氧气$\frac{\underline{\;点燃\;}}{\;}$三氧化二铝 | B. | 氢气+氧气$\frac{\underline{\;点燃\;}}{\;}$水 | ||
| C. | 甲烷+氧气$\frac{\underline{\;点燃\;}}{\;}$二氧化碳+水 | D. | 硫+氧气$\frac{\underline{\;点燃\;}}{\;}$二氧化硫 |
8.下列是某学生的一些实验操作或记录,其中正确的是( )
| A. | 用托盘天平称取12.05gNaCl固体 | |
| B. | 用100mL量筒取5.2mL稀硫酸 | |
| C. | 用pH试纸测得某种稀氢氧化钠溶液的pH为8.8 | |
| D. | 给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$ |
5.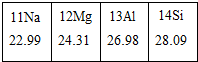 如图为元素周期表第三周期的一部分,下列说法中正确的是( )
如图为元素周期表第三周期的一部分,下列说法中正确的是( )
 如图为元素周期表第三周期的一部分,下列说法中正确的是( )
如图为元素周期表第三周期的一部分,下列说法中正确的是( )| A. | Si元素的名称是硅,其核电荷数为4 | |
| B. | Na的原子质量为22.99g | |
| C. | 镁原子在化学变化中易得到两个电子 | |
| D. | Al是地壳中含量最高的金属元素 |
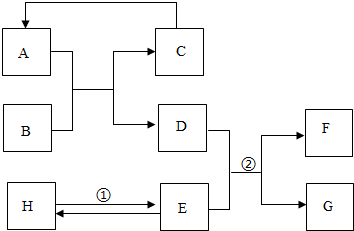
 .
.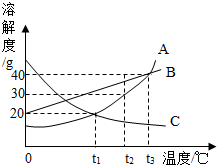 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.