题目内容
18.科学探究离不开化学实验,根据下列实验装置,回答问题:
(1)写出一种实验室用A装置制取气体的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,检验该气体的方法是伸入带火星的木条,若复燃,证明是氧气.
(2)某同学用碳酸钠粉末和稀盐酸制取二氧化碳,发生装置最好选择C而不选用B的原因是C装置的分液漏斗能控制反应速率,欲收集到干燥的二氧化碳所选装置的接口顺序为cda.(填写小写字母)
(3)该同学对(2)中实验后的液体溶质进行探究.请你与他一起完成以下探究活动:
【提出问题】溶液中的溶质是什么?
【猜想】猜想Ⅰ:NaCl; 猜想Ⅱ:NaCl和HCl; 猜想Ⅲ:NaCl和Na2CO3.
【实验】该同学选用了一种有色溶液进行探究,并证明了猜想Ⅲ是正确的结论.
请将猜想Ⅲ补充完整,并说出该同学所做的实验操作及现象.
(4)该同学欲测定碳酸钠的纯度,取12g样品配成50g溶液,加入足量氯化钙溶液,将产生沉淀过滤、洗涤、干燥,称得质量为10g,求碳酸钠样品的纯度.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气的检验方法是:将带火星的木条伸入集气瓶中,木条复燃,证明是氧气.某同学用碳酸钠粉末和稀盐酸制取二氧化碳,发生装置最好应选择C,因为碳酸钠是粉末,反应的速度快,分液漏斗可以控制反应的速度,二氧化碳可以用浓硫酸干燥,并且长进短出;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.碳酸钠与盐酸反应生成氯化钠和水和二氧化碳,反应后溶液中的溶质是什么呢,如果恰好完全反应溶质只有氯化钠;如果盐酸剩余,那么溶质是氯化钠和氯化氢;如果碳酸钠有剩余,那么溶质是氯化钠和碳酸钠;氯化钠显中性,碳酸钠显碱性,因此可以用紫色石蕊试液来检验,取少量反应后溶液,滴加入紫色石蕊溶液,变成蓝色证明猜想Ⅲ正确;有关化学方程式的计算要准确.
解答 解:(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,氧气的检验方法是:将带火星的木条伸入集气瓶中,木条复燃,证明是氧气;
(2)某同学用碳酸钠粉末和稀盐酸制取二氧化碳,发生装置最好应选择C,因为碳酸钠是粉末,反应的速度快,分液漏斗可以控制反应的速度,二氧化碳可以用浓硫酸干燥,并且长进短出;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;
(3)碳酸钠与盐酸反应生成氯化钠和水和二氧化碳,反应后溶液中的溶质是什么呢,如果恰好完全反应溶质只有氯化钠;如果盐酸剩余,那么溶质是氯化钠和氯化氢;如果碳酸钠有剩余,那么溶质是氯化钠和碳酸钠;氯化钠显中性,碳酸钠显碱性,因此可以用紫色石蕊试液来检验,取少量反应后溶液,滴加入紫色石蕊溶液,变成蓝色证明猜想Ⅲ正确;故答案为:猜想Ⅲ:NaCl和Na2CO3;取少量反应后溶液,滴加入紫色石蕊溶液,变成蓝色证明猜想Ⅲ正确;
(4)解:设10g样品中中Na2CO3的质量为x
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100
x 10g
$\frac{106}{x}$=$\frac{100}{10g}$
x=10.6g
样品中碳酸钠质量分数为:$\frac{10.6g}{12g}$×100%=88.3%.
故答案为:(1)2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,伸入带火星的木条,若复燃,证明是氧气;
(2)C装置的分液漏斗能控制反应速率;cda;
(3)NaCl和Na2CO3;
(4)88.3%.
点评 本考点主要考查了气体的检验、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关化学方程式的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

| A. | 用托盘天平称取12.05gNaCl固体 | |
| B. | 用100mL量筒取5.2mL稀硫酸 | |
| C. | 用pH试纸测得某种稀氢氧化钠溶液的pH为8.8 | |
| D. | 给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$ |
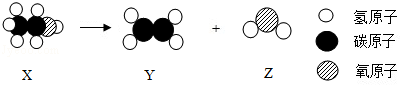
| A. | X、Y、Z都是有机物 | B. | X中碳、氢元素的质量比是1:3 | ||
| C. | X可由淀粉转化得到 | D. | Y是最简单的有机化合物 |
| A | B | C | D |
| 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | 在含有氯化铁的稀盐酸中加入氢氧化钠 | 两份质量和浓度都相同的H2O2溶液在有无MnO2的情况下,产生O2的质量与时间t的关系 | 在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  | 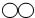 |  |  |
| A. | 反应前后各元素的化合价都不变 | |
| B. | 只有丙物质属于单质 | |
| C. | 反应物的分子总数不等于生成物的分子总数 | |
| D. | 该反应中含硫元素的化合物有两种 |
 向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )| A. | 0-a段只生成氢氧化铜沉淀 | |
| B. | 室温下,b点溶液的pH>7 | |
| C. | c点溶液中溶质至少有两种 | |
| D. | 整个过程中,溶液中氢元素的质量一直在增加 |
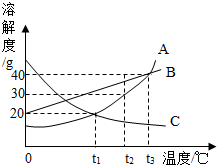 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.