题目内容
17.钙元素与人类生产、生活密切相关.(1)某品牌牙膏中摩擦剂的主要成分为碳酸钙,碳酸钙属于盐(填“酸”、“碱”、“盐”或“氧化物”)
碳酸钙作牙膏中的摩擦剂,利用碳酸钙的性质是②③(填序号).
①白色 ②难溶于水 ③硬度较大 ④热稳定性差
(2)硝酸钙是重要的化学试剂和化工原料.
①以大理石为原料制备硝酸钙的化学方程式为CaCO3+2HNO3=CaNO3+H2O+CO2↑.从硝酸钙的浓溶液中提取硝酸钙的操作方法是降温结晶(已知硝酸钙的溶解度随温度升高而增大).
②某实验需要500g质量分数为20%的硝酸钙溶液,配制该溶液需要硝酸钙的质量为100g;若用该溶液配制质量分数为5%的硝酸钙溶液,则该硝酸钙溶液与蒸馏水的质量之比为1:3.
分析 (1)根据碳酸钙的组成来分析类别,根据碳酸钙的性质来分析;
(2)①碳酸钙与硝酸反应生成硝酸钙和水和二氧化碳;硝酸钙的溶解度随温度升高而增大,从硝酸钙的浓溶液中提取硝酸钙的可以选择降温结晶;
②根据溶质的质量=溶液质量×溶质的质量分数,根据加水稀释溶质质量不变来分析.
解答 解:(1)碳酸钙是由金属钙离子和碳酸根离子组成的;碳酸钙作牙膏中的摩擦剂,利用碳酸钙的②难溶于水 ③硬度较大;答案:盐;②③;
(2)①大理石的主要成分碳酸钙与硝酸反应生成硝酸钙和水和二氧化碳;由于硝酸钙的溶解度随温度升高而增大,所以从硝酸钙的浓溶液中提取硝酸钙的操作方法降温结晶,
②硝酸钙的质量为:500g×20%=100g;
设,若用该溶液配制质量分数为5%的硝酸钙溶液,需要硝酸钙溶液的质量为x,需要水的质量为y,
20%x=(x+y)5%
$\frac{x}{y}=\frac{1}{3}$
答案:①CaCO3+2HNO3=CaNO3+H2O+CO2↑;降温结晶;②100g;1:3.
点评 本题能很好的考查学生对知识的掌握和应用,及分析、解决问题的能力,难度不大,要据相关知识结合具体情景仔细分析解答.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
8.下列是某学生的一些实验操作或记录,其中正确的是( )
| A. | 用托盘天平称取12.05gNaCl固体 | |
| B. | 用100mL量筒取5.2mL稀硫酸 | |
| C. | 用pH试纸测得某种稀氢氧化钠溶液的pH为8.8 | |
| D. | 给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$ |
5.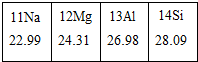 如图为元素周期表第三周期的一部分,下列说法中正确的是( )
如图为元素周期表第三周期的一部分,下列说法中正确的是( )
 如图为元素周期表第三周期的一部分,下列说法中正确的是( )
如图为元素周期表第三周期的一部分,下列说法中正确的是( )| A. | Si元素的名称是硅,其核电荷数为4 | |
| B. | Na的原子质量为22.99g | |
| C. | 镁原子在化学变化中易得到两个电子 | |
| D. | Al是地壳中含量最高的金属元素 |
12.下列变化过程中只发生了物理变化的是( )
| A. | 用铁矿石炼铁 | |
| B. | 由氮气合成氨 | |
| C. | 废气中的二氧化硫形成酸雨 | |
| D. | 二氧化碳气体经加压、降温得到干冰 |
2.以人为本,关注健康,是人类永恒的主题.下列叙述不正确的是( )
| A. | 过量补充碘元素,也会引起甲状腺肿大 | |
| B. | 硒、锌、铁、钠是人体所需的微量元素 | |
| C. | 禁止食用甲醛浸泡的黄豆芽、银鱼等食品 | |
| D. | 食用瘦肉、奶类、豆类都可以为人体补充蛋白质 |
9.X在一定条件下可转化为Y和Z,其反应的微观示意图如图.下列说法中正确的是( )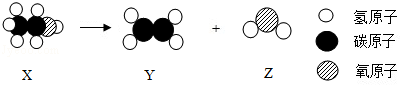
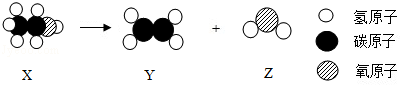
| A. | X、Y、Z都是有机物 | B. | X中碳、氢元素的质量比是1:3 | ||
| C. | X可由淀粉转化得到 | D. | Y是最简单的有机化合物 |
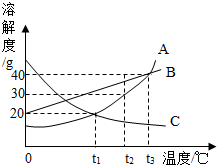 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.