题目内容
【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式_____,小明认为根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量。待镁条完全燃烧后,称量发现石棉网上的燃烧产物质量比反应前镁条质量还小,其主要原因是_____。
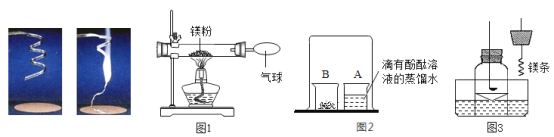
(2)小红按下图1装置改进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
提出问题:黄色固体是什么呢?
查阅资料:①氧化镁为白色固体;②镁条能在氮气中燃烧生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
做出猜想:黄色固体为Mg3N2
实验探究:按照图2所示,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B。当观察到_____现象时,可说明燃烧产物中含Mg3N2。
反思与交流:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理解释_____。
拓展延伸:为了证明镁可在氮气中燃烧生成氮化镁,小红又设计了如下方案进行验证:步骤①:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图3所示的装置;另准备一只有铜丝穿过的橡皮塞,铜丝末端固定一根镁条。
步骤②:引燃燃烧匙中足量的红磷,塞好橡皮塞,待充分冷却,观察到广口瓶内水面上升。
步骤③:往水槽中加水使广口瓶内外水面相平,点燃镁条,迅速更换橡皮塞,镁条在广口瓶内继续燃烧,放出热量,待冷却后广口瓶内水位继续上升。
(3)步骤②的目的是_____。
(4)写出镁在氮气中燃烧生成氮化镁的化学方程式_____
【答案】2Mg+O2![]() 2MgO 部分反应产物扩散到空气中 A中酚酞溶液变红 相同条件下,氧气的化学性质比氮气活泼 排除氧气的干扰 3Mg+N2
2MgO 部分反应产物扩散到空气中 A中酚酞溶液变红 相同条件下,氧气的化学性质比氮气活泼 排除氧气的干扰 3Mg+N2![]() Mg3N2
Mg3N2
【解析】
(1)镁条与氧气在点燃的条件下反应生成氧化镁,反应的化学方程式为:2Mg+O2![]() 2MgO;根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量,镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是部分反应产物扩散到空气中,即反应过程中部分氧化镁扩散到了空气中。故填:2Mg+O2
2MgO;根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量,镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是部分反应产物扩散到空气中,即反应过程中部分氧化镁扩散到了空气中。故填:2Mg+O2![]() 2MgO;部分反应产物扩散到空气中。
2MgO;部分反应产物扩散到空气中。
(2)[实验探究]如图,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B,实验过程中A中酚酞溶液变红,说明B中产生了氨气,进一步说明燃烧产物中含Mg3N2,故填:A中酚酞溶液变红;
[反思与交流]空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,这是因为相同条件下,氧气的化学性质比氮气活泼。
故填:相同条件下,氧气的化学性质比氮气活泼。
[拓展延伸](3)氧气可以和镁反应,所以要能够准确的判断出镁确实与氮气发生了反应,必须先排除氧气的干扰;故填:排除氧气的干扰;
(4)镁在氮气中燃烧生成氮化镁的化学方程为:3Mg+N2![]() Mg3N2.故填:3Mg+N2
Mg3N2.故填:3Mg+N2![]() Mg3N2。
Mg3N2。

【题目】将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应,测得反应前后各物质质量如下表所示,则下列说法错误的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 6.4 | 3.2 | 4.0 | 2.5 |
反应后的质量/g | 3.8 | 待测数据 | 7.2 | 2.5 |
A.上表中的“待测数据”的数值为0.6
B.甲和乙是反应物,丁可能是催化剂
C.该反应一定属于化合反应
D.丙物质与甲物质组成元素不一定相同
【题目】提出问题:蛋壳中的![]() 含量是多少呢?称取
含量是多少呢?称取![]() 蛋壳设计了以下的实验方案如图所示的实验装置。
蛋壳设计了以下的实验方案如图所示的实验装置。
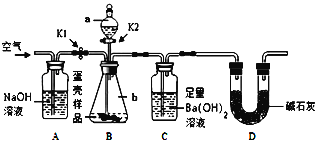
(实验步骤)
![]() 按如图连接好装置后,并______;
按如图连接好装置后,并______;
![]() 向B装置中加入蛋壳样品后,先通入空气一会儿;
向B装置中加入蛋壳样品后,先通入空气一会儿;
![]() 接下来的实验操作是______,直到______为止
接下来的实验操作是______,直到______为止![]() 填实验现象
填实验现象![]() ;
;
![]() 再通入空气一会儿,至装置C中不再产生沉淀为止;
再通入空气一会儿,至装置C中不再产生沉淀为止;
![]() 将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;![]() 重复上述实验。
重复上述实验。
(实验数据)重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量 |
|
|
|
(实验分析及数据处理)
![]() 上述数据能否用托盘天平称量______。
上述数据能否用托盘天平称量______。![]() 填“能”或“不能”
填“能”或“不能”![]()
![]() 若无A装置,直接通入空气,则测定结果将______。
若无A装置,直接通入空气,则测定结果将______。![]() 填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变”![]() 装置的作用是______。
装置的作用是______。
![]() 实验重复3次的目的是______。
实验重复3次的目的是______。
![]() 请利用3次实验数据的平均值,计算该蛋壳中的
请利用3次实验数据的平均值,计算该蛋壳中的![]() 质量分数是______。
质量分数是______。![]() 写出计算过程
写出计算过程![]()