题目内容
【题目】提出问题:蛋壳中的![]() 含量是多少呢?称取
含量是多少呢?称取![]() 蛋壳设计了以下的实验方案如图所示的实验装置。
蛋壳设计了以下的实验方案如图所示的实验装置。
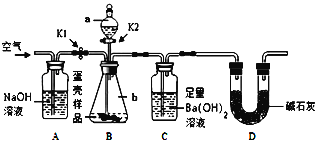
(实验步骤)
![]() 按如图连接好装置后,并______;
按如图连接好装置后,并______;
![]() 向B装置中加入蛋壳样品后,先通入空气一会儿;
向B装置中加入蛋壳样品后,先通入空气一会儿;
![]() 接下来的实验操作是______,直到______为止
接下来的实验操作是______,直到______为止![]() 填实验现象
填实验现象![]() ;
;
![]() 再通入空气一会儿,至装置C中不再产生沉淀为止;
再通入空气一会儿,至装置C中不再产生沉淀为止;
![]() 将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;![]() 重复上述实验。
重复上述实验。
(实验数据)重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量 |
|
|
|
(实验分析及数据处理)
![]() 上述数据能否用托盘天平称量______。
上述数据能否用托盘天平称量______。![]() 填“能”或“不能”
填“能”或“不能”![]()
![]() 若无A装置,直接通入空气,则测定结果将______。
若无A装置,直接通入空气,则测定结果将______。![]() 填“偏大”、“偏小”或“不变”
填“偏大”、“偏小”或“不变”![]() 装置的作用是______。
装置的作用是______。
![]() 实验重复3次的目的是______。
实验重复3次的目的是______。
![]() 请利用3次实验数据的平均值,计算该蛋壳中的
请利用3次实验数据的平均值,计算该蛋壳中的![]() 质量分数是______。
质量分数是______。![]() 写出计算过程
写出计算过程![]()
【答案】检验装置气密性 关闭![]() ,打开
,打开![]() ,加入稀盐酸 没有气泡产生 不能 偏大 防止空气中的二氧化碳进入装置C 减小实验误差
,加入稀盐酸 没有气泡产生 不能 偏大 防止空气中的二氧化碳进入装置C 减小实验误差 ![]() (详见解析)
(详见解析)
【解析】
实验步骤:
![]() 为防止装置漏气,影响实验效果,按如图连接好装置后,并检验装置气密性;
为防止装置漏气,影响实验效果,按如图连接好装置后,并检验装置气密性;
![]() 向B装置中加入蛋壳样品后,先通入空气一会儿;
向B装置中加入蛋壳样品后,先通入空气一会儿;
![]() 鸡蛋壳的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳。接下来的实验操作是关闭
鸡蛋壳的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳。接下来的实验操作是关闭![]() ,打开
,打开![]() ,加入稀盐酸,直到B中没有气泡产生为止;
,加入稀盐酸,直到B中没有气泡产生为止;
![]() 再通入空气一会儿,至装置C中不再产生沉淀为止;
再通入空气一会儿,至装置C中不再产生沉淀为止;
![]() 将装置C中的固、液混合物过滤、洗涤、烘干后称量其质量;
将装置C中的固、液混合物过滤、洗涤、烘干后称量其质量;![]() 重复上述实验。
重复上述实验。
实验分析及数据处理:
![]() 上述数据不能用托盘天平称量,原因是托盘天平的最小分度值是0.1g;
上述数据不能用托盘天平称量,原因是托盘天平的最小分度值是0.1g;
![]() 氢氧化钠会将空气中的二氧化碳吸收,所以无A装置,直接通入空气,空气中的二氧化碳会与氢氧化钡反应,测定结果将偏大;D装置的作用是防止空气中的二氧化碳进入装置C,影响,影响测量结果;
氢氧化钠会将空气中的二氧化碳吸收,所以无A装置,直接通入空气,空气中的二氧化碳会与氢氧化钡反应,测定结果将偏大;D装置的作用是防止空气中的二氧化碳进入装置C,影响,影响测量结果;
![]() 实验重复3次的目的是多次测量求平均值可以减小实验误差。
实验重复3次的目的是多次测量求平均值可以减小实验误差。
![]() 碳酸钡的质量为=
碳酸钡的质量为=![]() ;
;
设参加反应的碳酸钙的质量为x.。
根据化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,CO2 +Ba(OH)2 =BaCO3↓+ H2O,则有:

![]() x=10g ;
x=10g ;
该蛋壳中的![]() 质量分数=
质量分数=![]() 。
。