题目内容
【题目】请根据下图回答问题。
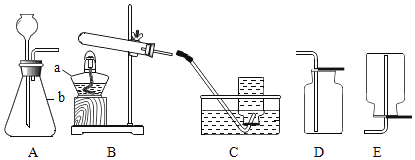
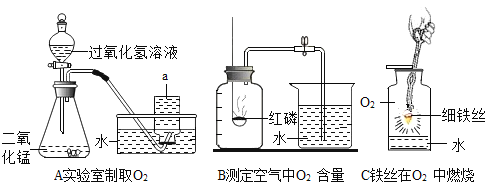
(1)图中仪器a的名称是_____、仪器b的名称是_____。
(2)用A与D相连可制取的一种气体是_____,该反应的化学方程式为_____。
(3)小明将B与C相连,用高锰酸钾制取氧气。实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装药品和放棉花 e.加热,收集氧气。上述过程中缺少的一步操作是_____,将该操作编号为f,则正确的操作顺序是_____。
(4)查阅资料:相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气。根据所查资料,制取氨气应选择的实验装置是_____(填序号)。
【答案】酒精灯 锥形瓶 二氧化碳(或氧气) CaCO3+2HCl=CaCl2+H2O+CO2↑(或2H2O2![]() 2H2O+O2↑) 检查装置的气密性 fdbeca BE
2H2O+O2↑) 检查装置的气密性 fdbeca BE
【解析】
(1)据图可知仪器a为酒精灯,b为锥形瓶;
(2)A装置与D装置连接可制取由固体和液体反应,生成的气体比密度大的气体,如二氧化碳、氧气等,制取氧气可用过氧化氢分解,不需加热,反应方程式是:2H2O2 ![]() 2H2O+O2↑,制取二氧化碳用大理石和稀盐酸混合制取,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+O2↑,制取二氧化碳用大理石和稀盐酸混合制取,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)用高锰酸钾制取氧气时,首先要检查装置的气密性,然后装入药品加热,收集气体,实验完成后要先撤导管,再停止加热;
(4)根据题意可知,制取氨气需要用加热固体的方法,故选择B装置,氨气(NH3)的密度比空气小,且易溶于水,故收集方法为向下排空气法。

【题目】小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃。那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水。用排水法收集氧气,恰好把5只集气瓶中的水排去。将带火星的木条依次插入①~⑤号瓶中,记录实验现象。
小亮在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见下表。
第一组 | 第二组 | 第三组 | |||||||||
集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
请根据实验回答下列问题:
(1)写出实验室用氯酸钾制取氧气的反应的符号表达式:_____。
(2)当收集的氧气占容积的体积分数最低为_____%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是_____%(计算结果保留整数)。
(3)根据以上的数据,你认为,使用带火星的木条验满氧气的方法是否可靠:_____(填“是”或“否”)。
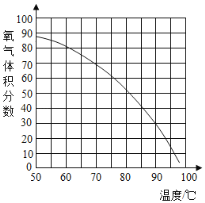
(4)用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸汽所致,此时混合气体中氧气的体积分数随温度变化的曲线如图所示。若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在_____℃。
(5)采取“半值法”探究能减少实验次数。
例如:第一组实验若按③、④的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在30%~40%之间,从而省去编号为①、②、⑤的实验。同理,第二组实验可以省去的实验编号为_____。