题目内容
7.钴(Co)是火箭发动机、导弹的部件和化工设备中各种高负荷的耐热部件以及原子能工业的重要金属材料,钴与铁的化学性质相似,都能与稀盐酸反应,在化合物中钴元素常显+2、+3价.下列说法正确的是(Co的相对原子质量为59)( )| A. | CoCl3读作“氯化亚钴” | |
| B. | CoCl3中钴元素的化合价为+2价 | |
| C. | 金属铜不能与CoCl2溶液发生反应 | |
| D. | CoCl2中钴元素的质量分数约为33.3% |
分析 A、根据化学式给物质命名;
B、根据化合物中正负化合价的代数和为0计算钴元素的化合价;
C、根据题意,金属钴(Co)与铁具有相似的化学性质,能够和盐酸反应,判断反应;
D、根据元素的质量分数公式计算.
解答 解:A、CoCl3读作“氯化钴”,故A说法错误;
B、CoCl3中氯元素的化合价为-1价,则钴元素的化合价为+3价,故B说法错误;
C、金属钴(Co)与铁具有相似的化学性质,能够和盐酸反应,说明Co位于氢前,因此Co的活动性比铜强,故铜不能和CoCl2溶液发生反应,故C说法正确;
D、CoCl2中钴元素的质量分数=$\frac{59}{59+35.5×2}$×100%≠33.3%,故D说法错误.
故选:C.
点评 本题属于信息题的考查,可以依据题目的信息结合相关的知识分析即可,难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
18.下列对有关实验现象或实验的描述正确的是( )
| A. | 铁丝在空气中燃烧时,火星四射,有黑色物质生成 | |
| B. | 石蜡在氧气中燃烧时,有水和二氧化碳生成 | |
| C. | 红热木炭放入盛有氧气的集气瓶中,剧烈燃烧,产生白烟 | |
| D. | 向硫酸铜溶液中滴加氢氧化钠溶液,出现浑浊现象 |
15.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如表所示.求:
(1)这瓶浓硫酸溶液的质量是多少克?其中含溶质多少克?
(2)若将这瓶浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少(计算结果保留到0.1%)
(3)欲配制500克质量分数为19.6%的稀硫酸,需要多少毫升这种浓硫酸?加水多少毫升?
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这瓶浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少(计算结果保留到0.1%)
(3)欲配制500克质量分数为19.6%的稀硫酸,需要多少毫升这种浓硫酸?加水多少毫升?
2.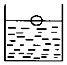 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )| A. | 加入少量硝酸钾晶体,充分搅拌 | B. | 蒸发一些溶剂,恢复到室温 | ||
| C. | 升高温度,使硝酸钾晶体析出 | D. | 降低温度,使硝酸钾晶体析出 |
12.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量稀硫酸 |
| C | NaCl溶液 | Na2CO3 | 适量硝酸钡溶液、过滤 |
| D | H2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
19.为了防止小包装食品受潮,在一些食品包装袋中放入的干燥剂是( )
| A. | 生石灰 | B. | 氢氧化钠 | C. | 浓硫酸 | D. | 无水硫酸铜 |
12.某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6
(1)所取的雨水是否为酸雨是(填“是”或“否”);在测定期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”)
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O
(3)为了防止“酸雨”的产生,保护我们的大自然,请提出一条合理化的建议:硫酸厂产生的尾气处理后再排放,煤燃烧前先脱硫.
(4)若用pH试纸测定雨水的酸碱度,测定方法是:用玻璃棒沾取雨水样品滴在pH试纸上,将pH试纸所显示的颜色与标准比色卡对比,读出数值.
| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
(1)所取的雨水是否为酸雨是(填“是”或“否”);在测定期间,雨水水样的酸性随着时间的变化逐渐增强(填“增强”或“减弱”)
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式:SO2+2NaOH═Na2SO3+H2O
(3)为了防止“酸雨”的产生,保护我们的大自然,请提出一条合理化的建议:硫酸厂产生的尾气处理后再排放,煤燃烧前先脱硫.
(4)若用pH试纸测定雨水的酸碱度,测定方法是:用玻璃棒沾取雨水样品滴在pH试纸上,将pH试纸所显示的颜色与标准比色卡对比,读出数值.
 氮化铝(AlN)是一种新型无机材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为:
氮化铝(AlN)是一种新型无机材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为: