题目内容
12.下列除去杂质的方法中正确的是( )| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量稀硫酸 |
| C | NaCl溶液 | Na2CO3 | 适量硝酸钡溶液、过滤 |
| D | H2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、KOH溶液能与适量稀硫酸反应生成硫酸钾和水,氯化钾不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、Na2CO3能与适量硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,故选项所采取的方法错误.
D、CO和H2均能与灼热的氧化铜反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:A.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
3.氯化钠是工业生产和生活的一种重要原料,也是实验室里常见的一种药品.下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
(1)计算第1次实验得到的氯化钠溶液的溶质质量分数.
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?
| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | m |
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?
7.钴(Co)是火箭发动机、导弹的部件和化工设备中各种高负荷的耐热部件以及原子能工业的重要金属材料,钴与铁的化学性质相似,都能与稀盐酸反应,在化合物中钴元素常显+2、+3价.下列说法正确的是(Co的相对原子质量为59)( )
| A. | CoCl3读作“氯化亚钴” | |
| B. | CoCl3中钴元素的化合价为+2价 | |
| C. | 金属铜不能与CoCl2溶液发生反应 | |
| D. | CoCl2中钴元素的质量分数约为33.3% |
17.下列说法不正确的是( )
| A. | 一切物质的化学性质都是在化学变化中表现出来的 | |
| B. | 铁合金、铜合金、铝合金不是纯净物 | |
| C. | 烧碱在水中电离出氢氧离子和钠离子,其水溶液呈电中性和碱性 | |
| D. | 加到水里的生石灰在反应前后质量和化学性质均不变 |
1.在实验室准备做粗盐提纯的实验时,其中过滤操作需要的仪器是( )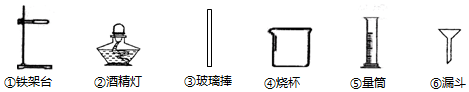

| A. | ①③④⑥ | B. | ①②③④⑥ | C. | ②③④ | D. | ④⑤⑥ |
17.对上述实验的分析,正确的是( )
| A. | 步骤①可省略 | |
| B. | 滤液Ⅲ中有三种溶质 | |
| C. | 滤渣乙的物质的量等于原固体混合物中氯化钾的物质的量 | |
| D. | 滤渣乙和滤渣戊的物质的量之和等于②中加入的硝酸银的物质的量 |
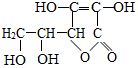 黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).
黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).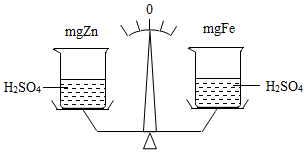 在调节好的天平两边的托盘里,各放质量相同的烧杯,分别盛放等量的同一种稀硫酸,天平仍然平衡,指针在O点.现分别向左边烧杯中加入m克锌,向右边烧杯中加入m克铁,如图所示.试回答:
在调节好的天平两边的托盘里,各放质量相同的烧杯,分别盛放等量的同一种稀硫酸,天平仍然平衡,指针在O点.现分别向左边烧杯中加入m克锌,向右边烧杯中加入m克铁,如图所示.试回答: