题目内容
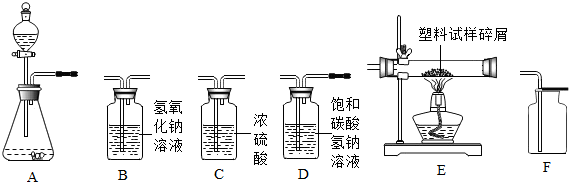
9.以下是一些制取气体的实验,请你一起参与探究.(1)某探究小组在实验室用如图所示装置制取气体.
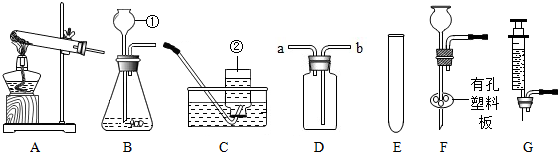
Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
| 编号 | 过氧化氢溶液质量/g | 催化剂质量/g | 待测数据 | |
| 实验1 | 50.0 | MnO2 | 0.2 | |
| 实验2 | 50.0 | CuO | X | |
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.
分析 长颈漏斗方便加液体药品,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.若用D装置进行排空气法收集二氧化碳,气体应从长管进入,因为二氧化碳的密度比空气大;检验二氧化碳已集满的方法是:把一个燃着的木条放在a管口处,木条熄灭,证明满了.由表格信息可知:表中X的数值应是0.2,因为控制变量法只能控制一个变量;表中的待测数据指单位时间内产生氧气的体积.
解答 解:(1)Ⅰ.长颈漏斗方便加液体药品,集气瓶是收集气体的仪器,故答案为:长颈漏斗;集气瓶;
Ⅱ.如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;如果用高锰酸钾制氧气就需要加热;故答案为:A;G;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从长管进入,因为二氧化碳的密度比空气大;检验二氧化碳已集满的方法是:把一个燃着的木条放在a管口处,木条熄灭,证明满了;故答案为:b;把一个燃着的木条放在a管口处,木条熄灭,证明满了;
(2)Ⅰ.由表格信息可知:表中X的数值应是0.2,因为控制变量法只能控制一个变量;故答案为:0.2;
Ⅱ.表中的待测数据指单位时间内产生氧气的体积,故答案为:D;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和催化剂的催化作用等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | 混合气体中一氧化碳质量为1.4g | |
| B. | 碱石灰增重质量为6.6g | |
| C. | 混合气体中碳、氢元素的质量比为9:2 | |
| D. | 混合气体中两种气体分子数之比为3:1 |
 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的 所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )| A. | HCl NaOH BaCl2 Na2SO4 | B. | H2SO4 Ba(OH)2 Na2SO4 BaCl2 | ||
| C. | HCl Ba(OH)2 Na2SO4 BaCl2 | D. | H2SO4 NaOH BaCl2 Na2SO4 |
药品,探究哪两种药品的反应适合在实验室制取CO2.请你参与探究并回答问题.
【提出问题】上述酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因是浓盐酸有挥发性.
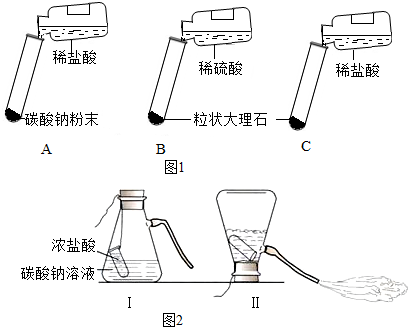
讨论后大家设计了如图1三个实验进行对比分析.
【实验与结论】
(1)请你填写实验报告中①、②处的内容.
| 实验 | 实验现象 | 实验结论 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①反应较强烈,产生大量气泡 | ②适宜制取二氧化碳 |
【拓展与迁移】
(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:操作简便.
(2)实验室制取二氧化碳,为了控制反应速率,可以采用哪种方式向反应容器中加入酸?用分液漏斗将酸滴加到反应容器中.
(3)图2是一种灭火器的工作原理示意图,其中用碳酸钠和浓盐酸反应来产生CO2的理由是反应剧烈,产生大量气泡,导致容器内部气压迅速增大.
| A. | 等于7 | B. | 小于7 | C. | 大于7 | D. | 无法确定 |