题目内容
20.根据给定元素及其化合价,按要求写出化学式或离子符号$\stackrel{+1}{H}$ $\stackrel{+1}{Na}$ $\stackrel{-1}{Cl}$ $\stackrel{-2}{O}$ $\stackrel{0}{N}$ $\stackrel{+6}{S}$ $\stackrel{+3}{Fe}$
①常见的酸HCl ②常见的碱NaOH③常见的盐NaCl.
④非金属氧化物H2O⑤气体单质N2.
⑥硫酸铁溶液中的主要阳离子是Fe3+;阴离子是SO42-.
分析 首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:①酸是指在电离时产生的阳离子全部是氢离子的化合物,根据提供的元素硝酸符合要求,其化学式为:HNO3.
②碱是指在电离时产生的阴离子全部是氢氧根离子的化合物,根据提供的元素氢氧化钠属于碱,其化学式为:NaOH;
③盐是由金属离子和酸根离子组成的化合物,根据提供的元素氯化钠属于盐,其化学式为:NaCl.
④非金属氧化物是只含有两种元素且其中一种元素是氧元素,另一种元素是非金属元素的化合物,根据提供的元素水、二氧化氮等符合题意,其化学式为:H2O;
⑤氮气属于气体单质.
⑥硫酸铁溶液中的主要阳离子是铁离子;阴离子是硫酸根离子.
故填:(1)HCl;(2)NaOH;(3)NaCl;(4)H2O;(5)N2;(6)Fe3+;SO42-
点评 本题难度不大,熟练掌握酸碱盐与单质的特征、组成及化学式的书写是正确解答此类题的关键所在.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
10.下列实验方案不可行的是( )
| A. | 用灼烧的方法区别腈纶制品和羊毛制品 | |
| B. | 用酚酞试液区分氢氧化钠溶液和碳酸钠溶液 | |
| C. | 用高温灼烧氧化铁和木炭粉混合物的方法制取少量铁 | |
| D. | 用加水溶解的方法区别NaOH、Na2SO4、NH4NO3三种白色固体 |
8.2.4g某纯净物完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 | |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| C. | 该物质一定含碳、氢、氧三种元素 | |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |
5.下列物质放入水中,能形成溶液的是( )
| A. | 碳酸钙 | B. | 植物油 | C. | 泥沙 | D. | 氯化钠 |
9.以下是一些制取气体的实验,请你一起参与探究.
(1)某探究小组在实验室用如图所示装置制取气体.
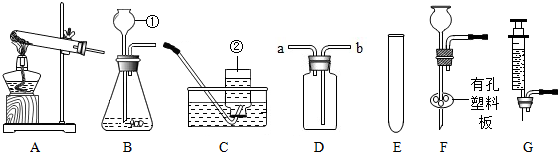
Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
I.表中X的数值应是0.2.
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.
(1)某探究小组在实验室用如图所示装置制取气体.

Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
| 编号 | 过氧化氢溶液质量/g | 催化剂质量/g | 待测数据 | |
| 实验1 | 50.0 | MnO2 | 0.2 | |
| 实验2 | 50.0 | CuO | X | |
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.

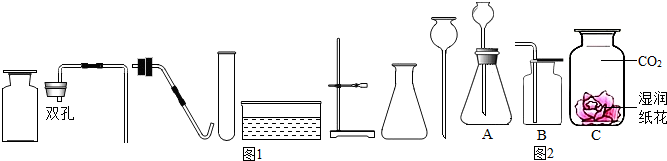
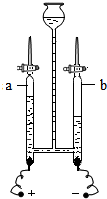 水在生活、生产和化学实验中起着十分重要的作有用.
水在生活、生产和化学实验中起着十分重要的作有用.