题目内容
17.有一混合气体,经测定只含有甲烷和一氧化碳,现将3.0g该混合气体在氧气中充分燃烧,并将生成物先后依次通过足量的浓硫酸和碱石灰,确保生成物被充分吸收,测得浓硫酸增重3.6g.则下列有关说法中不正确的是( )| A. | 混合气体中一氧化碳质量为1.4g | |
| B. | 碱石灰增重质量为6.6g | |
| C. | 混合气体中碳、氢元素的质量比为9:2 | |
| D. | 混合气体中两种气体分子数之比为3:1 |
分析 根据在化学反应中遵循质量守恒定律,即反应前后元素的种类、质量不变进行分析.
解答 解:A、根据题意“测得浓硫酸增重3.6g 则生成3.6克水”,因此氢元素的质量为:3.6g×$\frac{2}{18}$×100%=0.4g;此氢元素的质量,全部来自甲烷,则可知甲烷的质量为:0.4g÷($\frac{4}{16}$×100%)=1.6g.则一氧化碳质量为3.0g-1.6g=1.4g,故说法正确;
B、甲烷中碳元素的质量为(1.6g-0.4g)1.2g,一氧化碳中碳元素的质量为1.4g×$\frac{12}{28}$×100%=0.6g,即碳元素的质量为1.8g,因此产生二氧化碳的质量为1.8g÷
($\frac{12}{44}$×100%)=6.6g,因此碱石灰增重6.6g,故说法正确;
C、碳元素和氢元素的质量为1.8g:0.4g=9:2,故说法正确;
D、甲烷和一氧化碳的分子个数比为$\frac{1.6g}{16}$:$\frac{1.4g}{28}$=2:1,故说法错误;
故选项为:D.
点评 本题主要考查学生运用质量守恒定律解答问题的能力.运用质量守恒定律判断物质中含有的元素,是有关质量守恒定律的题目中常见的类型,解题的关键是正确理解质量守恒定律关于反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.2.4g某纯净物完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 | |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| C. | 该物质一定含碳、氢、氧三种元素 | |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |
5.下列物质放入水中,能形成溶液的是( )
| A. | 碳酸钙 | B. | 植物油 | C. | 泥沙 | D. | 氯化钠 |
2.甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如下所示:

根据如图所示微观示意图得出的结论中,正确的是( )

根据如图所示微观示意图得出的结论中,正确的是( )
| A. | 反应中含氢元素的化合物有三种 | |
| B. | 反应中甲和丙的质量之比为4:7 | |
| C. | 反应前后碳元素的化合价没有发生变化 | |
| D. | 水煤气的成分是一氧化碳和氧气 |
9.以下是一些制取气体的实验,请你一起参与探究.
(1)某探究小组在实验室用如图所示装置制取气体.
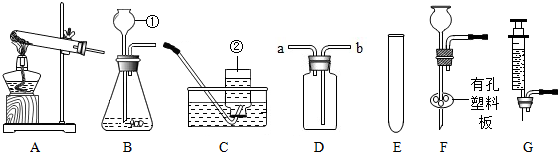
Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
I.表中X的数值应是0.2.
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.
(1)某探究小组在实验室用如图所示装置制取气体.

Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
| 编号 | 过氧化氢溶液质量/g | 催化剂质量/g | 待测数据 | |
| 实验1 | 50.0 | MnO2 | 0.2 | |
| 实验2 | 50.0 | CuO | X | |
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.
6.如表中除去物质中所含少量杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | 生石灰 | 石灰石 | 高温加强热 |
| B | 硫酸钠溶液 | 硫酸 | 加过量的碳酸钠溶液 |
| C | 铁 | 硫酸铜 | 加适量的水溶解、过滤、洗涤、干燥 |
| D | 二氧化碳 | 一氧化碳 | 将气体先通过足量的氢氧化钠溶液,再通过足量的浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
7.金属M是我们在研究金属活动性顺序时常用的一种金属单质,现将一定质量金属M的粉末加至含有H2SO4、MgSO4和CuSO4的混合溶液中,实验过程及现象如图所示,结合实际现象判断,得出的以下结论中,正确的是( )
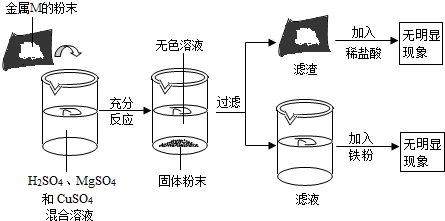

| A. | 金属M可能是单质铁 | B. | 滤渣中一定含有铜,可能含有金属M | ||
| C. | 滤液的质量大于原混合溶液的质量 | D. | 滤液中一定含有两种金属阳离子 |
 一天,小晨去郊游,在路上意外发现了几枚铜钱,上面有经色斑点.这些绿色斑点是怎么形成的?它的主要成分是什么?具有什么性质?围绕这些问题,她与同学们一起进行了如下探究活动:
一天,小晨去郊游,在路上意外发现了几枚铜钱,上面有经色斑点.这些绿色斑点是怎么形成的?它的主要成分是什么?具有什么性质?围绕这些问题,她与同学们一起进行了如下探究活动: