题目内容
1.如图所示为实验室常见气体制备,净化、干燥、收集和性质的部分仪器(组装实验装置时,可重复选择仪器).某学习两个化学实验探究小组的同学欲用他们完成各自的探究实验.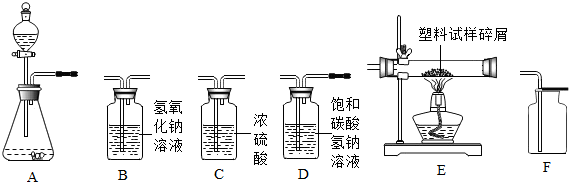
(1)第一组的同学以石灰石和稀盐酸为原料,在实验室中制备、收集干燥纯净的二氧化碳气体.按照要求设计实验装置、连接仪器,并检验装置的气密性.(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收).
①所选仪器的连接顺序为A→C→B→F(填写仪器序号字母).
①若将二氧化碳通入氢氧化钠溶液中,溶液的质量将增大(填“增大”“减小”“不变”之一),请解释原因二氧化碳气体被氢氧化钠溶液吸收后没有生成沉淀或气体.
(2)第二组的同学以过氧化氢溶液为和MnO2为原料制备氧气,并对某种塑料的组成元素进行分析探究(资料显示该塑料只含C,H,O三种元素).所选仪器按“A→C1→E→C2→B→碱石灰干燥管”的顺序连接,(C1,C2为浓硫酸洗气瓶),实验前检验装置气密性.使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
①仪器A中所发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③仪器E的玻璃管中放入的塑料试样碎屑质量为mg,塑料试样充分燃烧后,测得仪器C2质量增加ag,仪器B的质量增加bg,则mg该塑料试样中含氧元素的质量分数为(m-$\frac{3b}{11}$-$\frac{a}{9}$)g(计算结果可为分数形式).
③若装置中没有连接仪器C1,按照②测算出的该塑料试样中氧元素的质量与实际值比较将偏小(填“偏小”“偏大”“基本一致”之一).
分析 (1)①根据二氧化碳的性质可以知道干燥可以用浓硫酸,而吸收氯化氢气体可以用饱和的碳酸氢钠溶液,可以据此来解答该题;
②根据氢氧化钠溶液呈现碱性,二氧化碳与其反应产生碳酸钠和水,判断溶液质量的变化;
(2)①根据以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,产生水和氧气,写出反应的方程式;
②二氧化碳能和澄清的石灰水反应,仪器B增加的是二氧化碳的质量,根据二氧化碳的质量可求出二氧化碳中碳元素的质量;仪器C2质量增重是水的质量,根据生成水的质量计算出氢元素的质量.
③根据产生的氧气混有水蒸气,必须干燥,否则将使该塑料试样中氧元素的质量测算结果.
解答 解:(1)①以石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳,应该先选择固液反应的A装置作为发生装置,再通碳酸氢钠溶液除去氯化氢杂质,再通过浓硫酸吸水干燥,然后用向上排空气法收集,故连接的顺序为:A→C→B→F;故填:A;C;B;F;
②二氧化碳与氢氧化钠溶液反应产生碳酸钠和水,溶液的质量增加了;故填:增大;二氧化碳气体被氢氧化钠溶液吸收后没有生成沉淀或气体;
(2)①以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,产生水和氧气,反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②二氧化碳能使澄清的石灰水变浑浊.B装置增加的质量就是生成的二氧化碳的质量,二氧化碳中碳元素的质量=bg×$\frac{12}{44}$×100%=$\frac{3}{11}$bg;C2质量增加ag,;C2质量增加ag,这是生成水的质量,水中氢元素的质量为ag×$\frac{1×2}{18}×100%$=$\frac{1}{9}$ag;则塑料中含氧元素的质量为mg-$\frac{3}{11}$bg-$\frac{1}{9}$ag=(m-$\frac{3b}{11}$-$\frac{a}{9}$)g;故填:(m-$\frac{3b}{11}$-$\frac{a}{9}$);
③仪器C1是吸收氧气中的水蒸气,若没有该装置,会使仪器C2增重的质量偏大,即水的质量增加,因此测算出的该塑料试样中氧元素的质量与实际值比较将偏小.
故答案为:偏小.
点评 本题考查了常见气体的制取、干燥、除杂、收集及反应原理的书写等.综合性较强,在利用氧气的性质测定塑料的组成元素时,要注意区分各步操作的作用和目的,利用质量守恒定律进行相关问题的分析.

 阅读快车系列答案
阅读快车系列答案(1)某探究小组在实验室用如图所示装置制取气体.
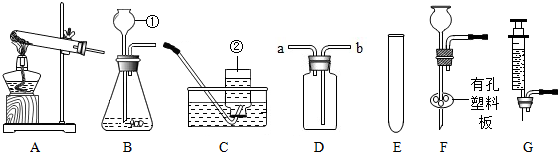
Ⅰ.写出仪器的名称:①长颈漏斗,②集气瓶;
Ⅱ.实验室如果用KMn04制取氧气所选择的发生装置为A;
实验室还可用二氧化锰与双氧水制取氧气,若要较好地控制产生氧气的速度,可以从E〜G中选取G(选填序号)组装成新的气体发生装置;写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.若用D装置进行排空气法收集二氧化碳,气体应从b(填“a”或“b”)端通人,检验二氧化碳已集满的方法是把一个燃着的木条放在a管口处,木条熄灭,证明满了
(2)为探究催化剂的种类对过氧化氢分解速度的影响,在相同条件下,同学们按如表进行实验并记录相关数据.(其他影响实验的因素均相同)
| 编号 | 过氧化氢溶液质量/g | 催化剂质量/g | 待测数据 | |
| 实验1 | 50.0 | MnO2 | 0.2 | |
| 实验2 | 50.0 | CuO | X | |
Ⅱ.表中的待测数据指D(填字母序号).
A.氧气的质量B.单位时间内产生氧气的质量
C.氧气的体积D.单位时间内产生氧气的体积.
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | 生石灰 | 石灰石 | 高温加强热 |
| B | 硫酸钠溶液 | 硫酸 | 加过量的碳酸钠溶液 |
| C | 铁 | 硫酸铜 | 加适量的水溶解、过滤、洗涤、干燥 |
| D | 二氧化碳 | 一氧化碳 | 将气体先通过足量的氢氧化钠溶液,再通过足量的浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 用灼烧的方法鉴别棉花和蚕丝 | |
| B. | 用燃着的木条鉴别氮气与二氧化碳 | |
| C. | 用盐酸验证敞口放置的NaOH溶液已变质 | |
| D. | 用碘水鉴别淀粉和葡萄糖 |
| A. | 在化学反应中,分子可分,原子也可分 | |
| B. | 配制稀硫酸时,将浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌 | |
| C. | 浓盐酸和浓硫酸敞口放于空气中,一段时间后溶液的质量会变小 | |
| D. | 氢氧化钠易潮解,可吸取空气中的水蒸气,所以可作为食品干燥剂 |
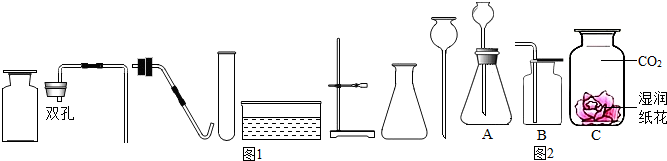
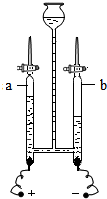 水在生活、生产和化学实验中起着十分重要的作有用.
水在生活、生产和化学实验中起着十分重要的作有用.