题目内容
7.物质发生化学变化的前后,总质量是否发生改变?是增加、减少还是不变?小刚、小莉按下面的步骤进行探究:(1)提出假设:物质发生化学变化的前后总质量不变.
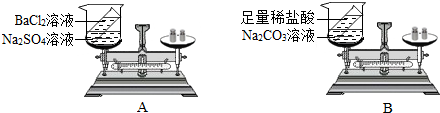
(2)设计并进行实验:小刚设计的实验装置如图A所示,选用的药品是BaCl2溶液和 Na 2SO4溶液(两者反应生成硫酸钡沉淀和氯化钠溶液);小莉设计的实验装置如图B所示,选用的药品是足量的稀盐酸和 Na2CO3溶液.他们在反应前后都进行了规范的操作、正确的称量和细致的观察.
①两个实验所发生反应的化学反应方程式为:
小刚的实验是:BaCl2+Na2S04=BaS04↓+2NaCl;
小莉的实验是:Na2C03+2HCl=2NaCl+H20+C02↑.
②实验结论:
小刚认为:在化学反应前后,生成物的总质量与反应物的总质量是相等的;
小莉认为:在化学反应前后,生成物的总质量与反应物的总质量是不相等的.
你认为小刚的结论正确,导致另一个实验结论错误的原因是:小莉的实验漏掉生成物的气体的质量,将反应物放在密闭容器中进行;
③请从原子的角度分析你认为正确结论的原因是:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;
④使用上述实验装置,请你选择另外两种药品进行实验达到实验目的,这两种药品可以是NaCl和AgNO3(填化学式)【注:以上四种药品均不能再用】.
分析 ①书写化学方程式时要注意反应物和生成物的化学式,并且不要忘记配平和生成物状态符号.
②在表达质量守恒定律时,一定不要漏掉反应物或生成物的质量,特别是气体物质,容易忽略.
③从原子的角度解释质量守恒定律,主要是原子的种类,数目,质量都不改变角度分析.
④选择另外两种药品验证质量守恒定律时,除了两种物质要反应外,最好不生成气体物质.
解答 解:①书写化学方程式为:BaCl2+Na2S04=BaS04↓+2NaCl,Na2C03+2HCl=2NaCl+H20+C02↑;
②小刚的结论是正确的,因为在质量守恒定律中,反应物的总质量等于生成物的总质量,小莉的实验中反应后生成的气体逸散到空气中去了,可将反应物放在密闭容器中进行实验.
③从原子的角度解释质量守恒定律,是因为反应前后原子的种类,数目,质量都不改变.
④选择药品验证质量守恒定律时,两种物质要能反应,最好不生成气体物质,故可以选NaCl、AgNO3.
答案:①BaCl2+Na2S04=BaS04↓+2NaCl; Na2C03+2HCl=2NaCl+H20+C02↑;
③小刚;小莉的实验漏掉生成物的气体的质量,将反应物放在密闭容器中进行.
④在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
⑤NaCl、AgNO3
点评 在验证质量守恒定律时,很容易忽略气体的质量,不管是反应物还是生成物中气体的质量,有气体参加或生成的实验必须在密闭容器中进行,这点一定要注意到.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
12.实验是研究化学的重要方法,以下实验不正确的是( )
| A. | 用点燃的方法除去二氧化碳中混有的少量的一氧化碳 | |
| B. | 用带火星的木条鉴别氧气和空气 | |
| C. | 用碘水或碘酒检验火腿肠中是否含有淀粉 | |
| D. | 配制10%氯化钠溶液的一般步骤是:计算、称量、溶解 |
19.下列各物质中能直接由单质金属和酸反应制得的是( )
| A. | FeCl3 | B. | CuSO4 | C. | FeCl2 | D. | HgCl |
16.实验探究:比较凌晨森林公园的空气中二氧化碳和氧气的含量与日照后森林公园的空气中二氧化碳和氧气的含量.
| 比较项目 | 实验操作 | 实验现象 | 得出结论 |
| 二氧化碳的含量 | 将澄清石灰水分别滴入盛有凌晨的空气和日照后的空气的集气瓶中 | 凌晨的空气变浑浊,日照后的空气中现象不明显 | 凌晨的空气中二氧化碳的含量比日照后的空气中更 高 |
| 氧气的含量 | 将燃着的木条分别伸入盛有凌晨的空气和日照后的空气你的集气瓶中 | 凌晨的空气中的木条很快熄灭,日照后的空气中的木条能燃烧一会再熄灭 | 凌晨的空气中氧气的含量比日照后的空气中更低 |
