例1.下列化学实验基本操作中,正确的是 ( )
A.稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌
B.用量筒量取液体时,视线与量筒内液体保持水平
C.用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁
D.用托盘天平称量物体时,称量物放在左盘,砝码放在右盘
解析:题目立意:考查化学实验基本操作中量筒、滴管、托盘天平的使用方法。
例2.下列各图所示的实验方法、装置和操作有无错误,如果有,说明如何改正。

解析:考查倒入液体并稀释浓硫酸的操作及过滤、蒸发等操作。
例3.量取25ml液体,最好选用 ( )
A.10ml量筒 B.50ml量筒 C.20ml量筒 D.100ml量筒
解析:考查用量筒量取一定体积液体,应选择精确度高,量取次数少的量筒。
例4.某学生用托盘天平称量时,误将药品和砝码位置放颠倒了,待平衡时,称得药品质量读数为9.5g(1g以下用游码),则药品的实际质量为 ( )
A.9g B.10g C.8.5g D.8g
解析:考查学生正确使用托盘天平的技能。
例5.用下列装置连接成一套测定水的组成的实验装置。
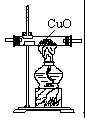 A.
A. |
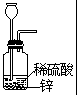 B.
B. |
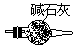 C.
C. |
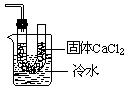 D.
D. |
(1)所用实验装置的连接顺序为_________________。 (2)装置C的作用是________________________,若不用C装置,测定出来的
氢元素与氧元素的质量比会___________(偏高或偏低)
(3)测量数据用m1、m2、m3、m4表示如下:
|
仪器名称 |
实验前 |
实验后 |
|
氧化铜和玻璃管 |
m1 |
m3 |
|
氯化钙和U形管 |
m2 |
m4 |
则在水中氢元素与氧元素的质量比是__________。 (4)如果在停止加热的同时,就停止了通入氢气,并拆开装置,则测定结果氢元素与氧
元素的质量比_________。(偏高或偏低)
解析:本实验是测定水中氢元素与氧元素的质量比,利用氢气还原氧化铜,生成水和铜测出氧化铜中的氧和生成水的质量,便可计算出水中氢元素与氧元素的质量比。首先制取氢气,为了防止生成的氢气中带有水蒸气,再将氢气通过盛有碱石灰的干燥管,吸收其中的水蒸气,将干燥的氢气通过受热的氧化铜,使氧化铜跟氢气反应生成的水再被盛有固体氯化钙的U形管在较低温条件下吸收,所以实验仪器的连接顺序应为B、C、A、D。生成的氢气如果不用C装置干燥,测出的水的质量即m4-m2的值偏高,这样测定出的氢元素与氧元素的质量比会偏高,因在生成的水中,所含氧元素的质量来自氧化铜中的氧元素质量,即m1-m3,这样便可知水中氢元素的质量,即(m4-m2)-(m1-m3)所以水中氢元素与氧元素的质量比为: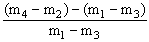 。如果在停止加热的同时,就停通入氢气,并拆开实验装置,其后果是使热的铜重新跟空气中的氧气反应,又生成氧化铜,这样测出的m3数值偏高,因而m1-m3的值偏低,使(m4-m2)-(m1-m3)的值偏高,导致
。如果在停止加热的同时,就停通入氢气,并拆开实验装置,其后果是使热的铜重新跟空气中的氧气反应,又生成氧化铜,这样测出的m3数值偏高,因而m1-m3的值偏低,使(m4-m2)-(m1-m3)的值偏高,导致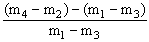 偏高,即此时会使水中的氢元素与氧元素的质量比偏高。
偏高,即此时会使水中的氢元素与氧元素的质量比偏高。