0 39077 39085 39091 39095 39101 39103 39107 39113 39115 39121 39127 39131 39133 39137 39143 39145 39151 39155 39157 39161 39163 39167 39169 39171 39172 39173 39175 39176 39177 39179 39181 39185 39187 39191 39193 39197 39203 39205 39211 39215 39217 39221 39227 39233 39235 39241 39245 39247 39253 39257 39263 39271 447348
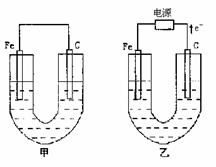 (1)若两池中均为
(1)若两池中均为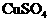 溶液,反应一段时间后
溶液,反应一段时间后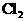 将生成的
将生成的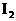 又氧化。若反应的
又氧化。若反应的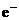 后停止实验,池中溶液体积是200mL,则溶液混匀后的pH=____。
后停止实验,池中溶液体积是200mL,则溶液混匀后的pH=____。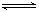 2C(g);DH<0
2C(g);DH<0
 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)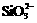 下列各组离子在指定条件下一定不能大量共存的是
下列各组离子在指定条件下一定不能大量共存的是 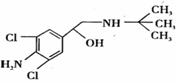 去年,某地区约 300 多人,因食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如右图,则它可能发生的化学反应有:
去年,某地区约 300 多人,因食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如右图,则它可能发生的化学反应有: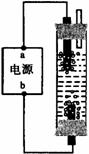 某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是