21. (12分)元素周期表是学习化学的重要工具,它包含了许多的信息和规律。下表是元素周期表的一部分,请从下表①-⑩十种元素中选择适当的元素回答下列问题:
|
族 周期 |
I A |
II A |
III A |
IV A |
V A |
VI A |
VII A |
|
1 |
① |
|
|||||
|
2 |
② |
③ |
④ |
|
⑤ |
⑥ |
|
|
3 |
|
⑦ |
⑧ |
|
|
⑨ |
⑩ |
(1)表中元素形成的四核10电子阳离子的化学式为 ,形成的四核18电子分子的化学式为_____。
(2)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质,写出元素③的氢氧化物与NaOH溶液反应的离子方程式___ _ ___。与元素⑦的性质相似的不同族元素是________(填元素符号)。
(3)某元素原子的次外层为2个电子,其最高正价与最低负价的代数和为2,则该元素的名称是____。另有一元素,其原子的核外电子数等于电子层数。这两种元素可以形成多种化合物,其中有一种离子化合物A中两元素的原子个数比为1:5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构。写出A的电子式 。A物质与水反应生成一种碱和无色气体,写出有关的化学方程式 ,该反应中的还原剂为 。
(4)物质熔沸点的高低与该物质的晶体结构有关。④的单质晶体熔点为2573K,沸点2823K,硬度大,则属于 晶体。某同学猜想⑧和⑩形成的化合物B晶体类型与NaCl相同,则B的熔沸点应 (填“高于”或“低于”)NaCl。如果用实验证明上述猜想不正确,你的实验方案是
。
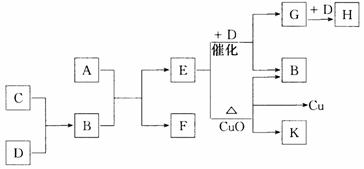
 2C(g)。已知加入1 mol
A和2 mol B且达到平衡后,生成了a mol C,此时C在平衡混合气体中的物质的量分数为a。在相同实验条件下,回答下列问题:
2C(g)。已知加入1 mol
A和2 mol B且达到平衡后,生成了a mol C,此时C在平衡混合气体中的物质的量分数为a。在相同实验条件下,回答下列问题: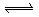 B+D在四种不同条件下进行B、D起始浓度为零,反应物A的浓度(mol/L),随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行B、D起始浓度为零,反应物A的浓度(mol/L),随反应时间(min)的变化情况如下表: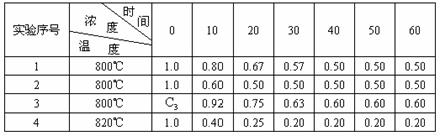
 ,实验1为
,实验1为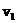 ,若相同时间内
,若相同时间内 ,理由是____________________
_____;
,理由是____________________
_____;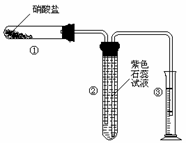 (2) 乙同学加热的是Cu(NO3)2。加热过程发现:装
(2) 乙同学加热的是Cu(NO3)2。加热过程发现:装  2Ag2O+4NO2↑+O2↑ (Ⅱ) 2AgNO3
2Ag2O+4NO2↑+O2↑ (Ⅱ) 2AgNO3