24.甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上常采用下列反应合成甲醇:CO(g) + 2H2(g)
 CH3OH(g)
ΔH1
CH3OH(g)
ΔH1
①下表所列数据是上述反应在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ;ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ;ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ;ΔH = -44.0 kJ/mol
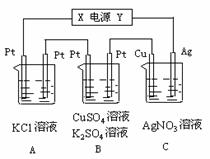 请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为 kJ。
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为 kJ。


 答题卷(请按要求写好姓名,班级和考号,只交答题卷)
答题卷(请按要求写好姓名,班级和考号,只交答题卷)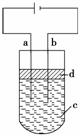 由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得