23.(6分)常压下,加热NaHCO3饱和溶液,测得溶液的pH变化如下表
|
温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液升温后pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,而Na2CO3的水解程度大小NaHCO3,所以pH升高。
丙同学设计如下方案探究甲、乙的判断。
(1)在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,乙判断正确。试剂X是
(填序号)。
A.Ba(OH)2溶液 B.BaC12溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则甲判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙确定 (填“甲”或“乙”)判断是错误的,理由是 。
 eC(g)+fD(g),在反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列叙述正确的是( )
eC(g)+fD(g),在反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图所示。下列叙述正确的是( )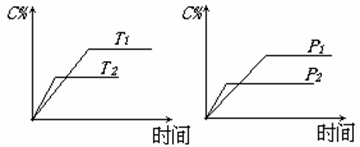
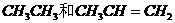 B.
B.
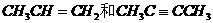
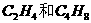 D.
D.
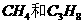
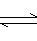 CH3COO-+H3O+ B.CO2+H2O
CH3COO-+H3O+ B.CO2+H2O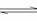 HCO3-+OH-
D.HS-+H2O
HCO3-+OH-
D.HS-+H2O S2-+H3O+
S2-+H3O+