21、(9分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、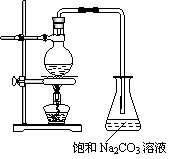 纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH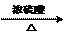 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)若用右图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为:__________________________、______________________________等。
(2)此反应以浓硫酸为催化剂,可能会造成____________、_________等问题。
(3)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
|
同一反应时间 |
同一反应温度 |
||||
|
反应温度/℃ |
转化率(%) |
选择性(%) |
反应时间/h |
转化率(%) |
选择性(%) |
|
40 |
77.8 |
100 |
2 |
80.2 |
100 |
|
60 |
92.3 |
100 |
3 |
87.8 |
100 |
|
80 |
92.6 |
100 |
4 |
92.3 |
100 |
|
120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
|
选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列__________(填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
②当反应温度达到120℃时,反应选择性降低的原因可能为__________。
(3)请设计实验方案进一步确定该固体混合物的组成。叙述实验操作、预期现象和结论。
[提示]Ⅰ、在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ、注意文字简洁,确保不超过答题卡空间,可以不填满。
|
实验操作 |
预期现象和结论 |
|
|
|
|
|
|
20.(11分)向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在2支试管中分别加入10mL等浓度的草酸溶液,在①号瓶中加入少量硫酸锰固体。然后在两支试管中加入0.1 mol·L-1的高锰酸钾溶液现象如下(表1)
|
加入药品 |
不加硫酸锰的硫酸酸化的草酸溶液 |
加少量硫酸锰的硫酸酸化的草酸溶液 |
|
实验现象(褪色时间) |
草酸褪色很慢(30s) |
草酸褪色很快(2s) |
实验(2):在2支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后加入5滴0.1 mol·L-1的高锰酸钾溶液。现象如下(表2)
|
编号 |
①号试管 |
②号试管 |
|
褪色时间 现象 |
100
s |
90
s |
|
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
|
编号 |
①号试管 |
②号试管 |
③号试管 |
|
褪色时间 实验现象 |
90
s |
100
s |
120
s |
|
均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
(1) 该研究性学习小组提出猜想与假设的理论依据是(从化学反应原理的角度作答): 。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫 法;
(3)设计实验(1)对应的假设是 ;
实验(1)得出的结论是 。
(4)由实验(2)和实验(3)得出的结论是 ;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液的离子方程式:
。
16.某些烃的燃烧热(kJ/mol)如下表,下列表示正确的是AB
|
化合物 |
燃烧热 |
化合物 |
燃烧热 |
|
甲烷 |
891.0 |
正丁烷 |
2878.0 |
|
乙烷 |
1560.8 |
异丁烷 |
2869.6 |
|
丙烷 |
2221.5 |
2-甲基丁烷 |
3531.3 |
|
乙烯 |
1411.0 |
乙炔(C2H2) |
1300.0 |
A.热稳定性:正丁烷<异丁烷
B.乙烷燃烧的热化学方程式C2H6(g)+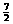 O2(g)=2CO2(g)+3H2O(l);∆H=-1560.8kJ/mol
O2(g)=2CO2(g)+3H2O(l);∆H=-1560.8kJ/mol
C.等物质的量的乙烯和乙炔(C2H2)完全燃烧,乙烯放出的热量多,故用氧烯焰来切割或焊接金属比氧炔焰好
D.相同质量的烃、碳的质量分数越大,燃烧放出的热量越多