0 24780 24788 24794 24798 24804 24806 24810 24816 24818 24824 24830 24834 24836 24840 24846 24848 24854 24858 24860 24864 24866 24870 24872 24874 24875 24876 24878 24879 24880 24882 24884 24888 24890 24894 24896 24900 24906 24908 24914 24918 24920 24924 24930 24936 24938 24944 24948 24950 24956 24960 24966 24974 447348
 B.
B.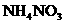
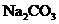 D.
D.

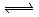
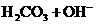





 的溶液
的溶液 的溶液 D.
的溶液 D. 的氢氧化钡溶液
的氢氧化钡溶液 B.
B. D.
D.
 B.NO C.
B.NO C.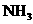 D.
D.
 B.CO C.
B.CO C. D.
D. A.碳酸钠固体
B.水 C.硫酸钾溶液
D.硫酸铵固体
A.碳酸钠固体
B.水 C.硫酸钾溶液
D.硫酸铵固体 4NO + 6H2O(g)
4NO + 6H2O(g) 2C(气),两秒种后反应速率如下
2C(气),两秒种后反应速率如下 2NH3+Q2,反应速度为v 2。当温度升高时,v 1和v 2的变化情况为( )
2NH3+Q2,反应速度为v 2。当温度升高时,v 1和v 2的变化情况为( )