24.在390 ℃,3.03×105 Pa下,以CO和H2为原料合成CH3OH,存在下列平衡:CO(气)+H2(气) ?CH3OH(气),当原料中H2和CO的比例不同时,对CO的转化率及平衡混合物中甲醇的含量都有影响。
(1)以m表示H2和CO的物质的量之比,(即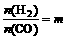 ),a表示CO的转化率,y为平衡时混合物中CH3OH的体积分数,试推断m,a,y三者的关系。
),a表示CO的转化率,y为平衡时混合物中CH3OH的体积分数,试推断m,a,y三者的关系。
(2)下表列出m=1,2,3,4时的一部分实验数据,试填出格中 a与y之值:
|
m |
1 |
2 |
3 |
4 |
|
a |
0.25 |
0.45 |
|
|
|
y |
|
|
19.35% |
16.35% |
(3)根据以上计算数据讨论:反应物比例对平衡混合物中CH3OH含量的影响,并选择一最佳比例。
21.下表数据是在某温度下,金属镁和镍分别在O2中进行氧化反应时,在金属表面生成氧化薄膜的实验记录:
|
反应时间t/n |
1 |
4 |
9 |
16 |
25 |
|
MgO层厚y/nm |
0.05 a |
0.20 a |
0.45 a |
0.80 a |
1.25 a |
|
NiO层厚y’/nm |
b |
2 b |
3 b |
4 b |
5 b |
注:a和b均为与温度有关的常数。
请填空回答:
(1)金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是_________。
(2)金属氧化膜的膜厚y跟时间t所呈现的关系是(填直线型,抛物线型,对数或双曲线等类型):MgO氧化膜厚y属______型,NiO氧化膜厚y’属______型。
(3)Mg和Ni比较,哪一种金属更具有耐腐蚀性______,其理由是______________。
19.在10℃和2×105 Pa的条件下,反应aA(气)?d D(气)+eE(气)建立平衡,再逐步增加体系的压强(温度保持不变),下表表示不同压强下的反应建立平衡时物质D的浓度:
|
压强/Pa |
2×105 |
5×105 |
1×106 |
|
D的浓度/(mol/L) |
0.085 |
0.20 |
0.44 |
(1)压强从2×105增加到5×105 Pa时,平衡向_____方向移动,理由是_______。
(2)压强从2×105增加到1×106 Pa时,平衡向_____方向移动,理由是_______,平衡之所以向该方向移动,这是由于____________。
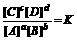 ,K为平衡常数。现有一反应:CO(气)+H2O(气)?CO2(气)+H2(气)+Q,在85 ℃时,K=1。
,K为平衡常数。现有一反应:CO(气)+H2O(气)?CO2(气)+H2(气)+Q,在85 ℃时,K=1。