27. (8分)下图是元素周期表中的前四周期,①-⑨为相应的元素,请从中选择合适的元素回答问题:
|
① |
|
|
|||||||||||||||
|
|
|
|
② |
③ |
④ |
⑤ |
⑥ |
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
⑦ |
|
|
⑧ |
⑨ |
|
|
|
|
|
|
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,①元素位于周期表的 区。
(2)②、⑥两元素形成的化合物的空间构型为 ,其中心原子的杂化轨道类型为 。
(3)写出元素⑧基态原子的电子排布式 。
(4)⑧的二价阳离子与过量的④的氢化物的水化物作用的离子方程式为: 。
(5)元素⑦与CO可形成的 X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于 晶体(填晶体类型)。
(6)元素⑨的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为 。
(7) 金属⑦的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。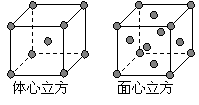 则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为 。
则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为 。
25.(8分)已知元素的电负性和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素电负性的数值:
|
元素 |
Al |
B |
Be |
C |
Br |
F |
Li |
|
电负性 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
|
元素 |
Mg |
Na |
O |
P |
S |
Si |
|
|
电负性 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
|
试结合元素周期律知识完成下列问题:
(1)试推断AlBr3、Na F中的化学键类型分别是 、 。
(2)根据上表给出的数据,简述主族元素电负性的数值大小与元素的金属性或非金属性强弱之间的关系______________________________;简述第二周期元素(除惰性气体外)电负性的数值大小与原子半径之间的关系___________________。
(3)请你预测Br与I元素的电负性的大小关系Br____I。
(4)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于______原子(填元素符号)。
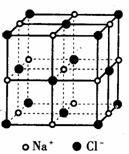
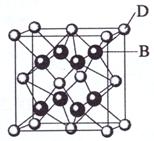 (15分)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B是所有元素中电负性最大的元素。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第6列元素。D的原子序数比E小4,D跟B可形成离子化合物其晶胞结构如右图。
(15分)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B是所有元素中电负性最大的元素。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第6列元素。D的原子序数比E小4,D跟B可形成离子化合物其晶胞结构如右图。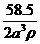 B.
B.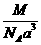 C.
C. 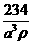 D.
D. 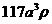
 B.第一电离能Y一定小于X
B.第一电离能Y一定小于X