22.(16分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)

|
|
|
|
 A B C
A B C
试回答下列问题:
(1)若X是强氧化性气体单质,则A可能是 ________________(填序号)
a.C b.Al c.Na d.Mg
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在A中燃烧产生棕黄色的烟
①B的化学式为________________,C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)________________________________________。
②向C的溶液中加入氢氧化钠溶液,现象是_______________________________,涉及的氧化还原反应的化学方程式为__________________________________。
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱,则B的化学式为________,反应②的离子方程式为_______________________________。
20.(16分)下列是关于Cl2的制备和性质的系列实验,请回答有关问题。
|
MnO2+4HCl(浓)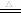 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
写出该反应的离子方程式_________________________________,指出该反应的还原剂:_________。产生11.2LCl2(标准状况),转移的电子物质的量是______。
(2)把红热的铜丝插入已收集满氯气的集气瓶中。
可观察的现象:_______________________________,
再往瓶中加入少量的水,振荡,溶液呈____色。该反应的化学方程式:______________,
(3)如果把干燥的氯气通入干燥的有色布条中,布条_____褪色,
(4)多余的氯气要用氢氧化钠溶液吸收,
写出该反应的离子方程式:_______________________________________,
(5)Cl2有____,该实验应在通风橱中进行。