网址:http://m.1010jiajiao.com/timu3_id_206586[举报]
(1)实验室是用二氧化锰和浓盐酸反应制氯气,其化学方程式是:MnO2+4HCl(浓)
| ||
写出该反应的离子方程式
(2)把红热的铁丝插入已收集满氯气的集气瓶中.
可观察的现象:
(3)如果把干燥的氯气通入干燥的有色布条中,布条
(4)多余的氯气要用氢氧化钠溶液吸收,写出该反应的离子方程式:
(5)Cl2有
 下列是治疗口腔炎症的药物华素片(西地碘片)的部分使用说明:
下列是治疗口腔炎症的药物华素片(西地碘片)的部分使用说明:
| 使用说明书 | |
| 主要成分 | 活性分子碘含量:1.5mg/片 |
| 贮藏 | 遮光、密闭、在阴凉处保存 |
| 有效期 | 二年 |
(1)推断华素片______(填“是”或“不是”)白色.
(2)某同学欲证实该药片中确定含有分子碘,设计并完成如下实验:
①将药片研碎、溶解、过滤,所得滤液分装于甲、乙两支试管中备用.
②在甲试管中加入下列一种试剂,振荡、静置,观察到液体分层,上层液体颜色为______色,所加试剂为下列中的______,由此说明分子碘的存在.
A.苯 B.酒精 C.四氯化碳 D.盐酸
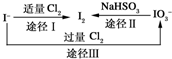
(3)碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如下转化关系:
①如以海水为原料制取I2,加入的Cl2要适量,如过量就会发生途径Ⅲ的副反应,在该反应产物中,IO3-与Cl-的物质的量之比为1:6,则氧化剂和还原剂的物质的量之比为______.
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应离子方程式是______. 查看习题详情和答案>>
| 使用说明书 | |
| 主要成分 | 活性分子碘含量:1.5mg/片 |
| 贮藏 | 遮光、密闭、在阴凉处保存 |
| 有效期 | 二年 |
(1)推断华素片______(填“是”或“不是”)白色.
(2)某同学欲证实该药片中确定含有分子碘,设计并完成如下实验:
①将药片研碎、溶解、过滤,所得滤液分装于甲、乙两支试管中备用.
②在甲试管中加入下列一种试剂,振荡、静置,观察到液体分层,上层液体颜色为______色,所加试剂为下列中的______,由此说明分子碘的存在.
A.苯 B.酒精 C.四氯化碳 D.盐酸
(3)碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如下转化关系:
①如以海水为原料制取I2,加入的Cl2要适量,如过量就会发生途径Ⅲ的副反应,在该反应产物中,IO3-与Cl-的物质的量之比为1:6,则氧化剂和还原剂的物质的量之比为______.
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应离子方程式是______.

(15分)高纯氧化铁(α—Fe2O3)是现代电子工业的重要材料。实验室用硫铁矿烧渣(主要成分为Fe2O3、FeO,还含有SiO2等杂质)为原料制备高纯氧化铁的步骤如下:

回答下列问题:
 (1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:
。
(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式:
。
(2)实验室欲用18.4mol·L-1的浓硫酸配制100mL 5.0mol·L-1的硫酸
溶液,所用的玻璃仪器胶头滴管、量筒、烧杯、玻璃棒外,还有
(填写仪器名称)。
(3)某同学用右图所示装置进行过滤操作。
①请指出其中的错误之处: ;
②过滤后,洗涤过滤器中少量沉淀的方法是 。
(4)某同学用下图所示装置(尾气吸收装置未画出)实验向溶液Y中通入NH3和CO2

①下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl b.CaCO3(块状) c.Ca(OH)2 d.NaOH
e.浓氨水 f.稀盐酸 g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为 和 (用药品序号填空);装置D处药品的最佳选择为 和 (用药品序号填空)。
②下列各项制备实验中,也可利用装置D处仪器完成的是 (填序号)。
A.MnO2与浓盐酸反应制备Cl2
B.Cu与浓硫酸反应生成SO2
C.由KMnO4分解制O2
D.乙醇与乙酸反应制备乙酸乙酯
E.Zn与稀硫酸反应制备H2
③写出上述装置A处的试管中所发生反应的化学方程式 。
④若通入一定量的NH3和CO2后,装置C处的溶液中只含有S、N、H、O四种元素。用pH试纸测定该溶液pH的方法是 ;若该溶液呈中性,则溶液中的NH+4和SO2-4的物质的量浓度间的数量关系为 。(离子的浓度用符号[NH+4]和[SO2-4]表示)
查看习题详情和答案>>
 下列是治疗口腔炎症的药物华素片(西地碘片)的部分使用说明:
下列是治疗口腔炎症的药物华素片(西地碘片)的部分使用说明:| 使用说明书 | |
| 主要成分 | 活性分子碘含量:1.5mg/片 |
| 贮藏 | 遮光、密闭、在阴凉处保存 |
| 有效期 | 二年 |
(1)推断华素片
(2)某同学欲证实该药片中确定含有分子碘,设计并完成如下实验:
①将药片研碎、溶解、过滤,所得滤液分装于甲、乙两支试管中备用.
②在甲试管中加入下列一种试剂,振荡、静置,观察到液体分层,上层液体颜色为
A.苯 B.酒精 C.四氯化碳 D.盐酸
(3)碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如下转化关系:
①如以海水为原料制取I2,加入的Cl2要适量,如过量就会发生途径Ⅲ的副反应,在该反应产物中,IO3-与Cl-的物质的量之比为1:6,则氧化剂和还原剂的物质的量之比为
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应离子方程式是