1、化学反应的基本类型比较
|
反应类型 |
概 念 |
特 征 |
举例 |
|
化合反应 |
由两种或两种以上的物质生成另一种物质的反应。 |
A+B→AB 多变一 |
S+ O2 SO2 SO2 |
|
分解反应 |
一种物质生成两种或两种以上其它物质的反应。 |
AB→A+B 一变多 |
2H2O电解2H2↑+O2↑ |
|
置换反应 |
一种单质跟一种化合物反应生成另一种单质和另一种化合物 |
A+BC→B+AC 一换一 |
HCl+ Zn= ZnCl2 + H2↑ |
|
复分解反应 |
两种化合物相互交换成分,生成两种新化合物的反应。 |
AB+CD→AD+BC 成分相交换 |
H2SO4+2NaOH =Na2SO4+2H2O |
3、物理变化与化学变化的区别和联系
|
|
物理变化 |
化学变化 |
|
概念 |
没有生成其他物质的变化 |
变化时生成了其他物质的变化 |
|
本质区别 |
宏观:没有其他物质生成 微观:构成物质的微粒不变,只是微粒间隔可能改变 |
宏观:有其他物质生成 微观:构成物质的微粒发生了变化,变成了另一种物质的微粒 |
|
外观区别 |
状态、形状、大小的改变 |
常伴随发光、放热、变色、生成气体、生成沉淀等。 |
|
举例 |
水的三态变化,汽油挥发 |
镁条燃烧、碱式碳酸铜分解 |
|
区分依据 |
有没有其他物质生成 |
|
|
联系 |
化学变化与物理变化往往同时发生,在化学变化中,同时发生物理变化;在物理变化中,不一定发生化学变化 |
[例1](2009·烟台)“民以食为天”。下列过程中发生了化学变化的是( )
A.淘米
B.洗菜
C.苹果榨汁 D.葡萄酿酒
[答案]D
[解析]淘米、洗菜是把米和菜中的杂质用水冲去,没有产生新物质,属于物理变化,苹果榨汁是苹果通过挤压的方式把其中所含的水分挤出,苹果汁本来就存在于苹果中,也没有产生新物质,属于物理变化,葡萄酿酒是通过发酵等多种程序,让葡萄中的有机物质转变为乙醇等新物质,所以属于化学变化。
[规律小结]物质的变化分为物理变化和化学变化,两者的区别在于有没有新物质生成,即发生化学变化的依据是产生了新物质。
变式训练一
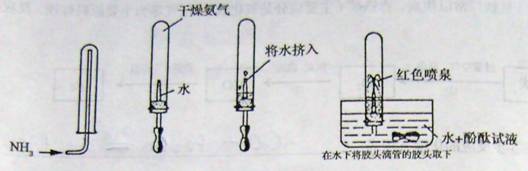 请根据上图中所示的信息,归纳出有关氨气的性质:
请根据上图中所示的信息,归纳出有关氨气的性质: