32.(12分)紫外线辐射可使细胞产生活性氧和自由基,二者极不稳定,容易发生一系列的氧化连锁反应,所产生的某些氧化产物可以对细胞造成伤害。一些水果的果皮富含抗氧化剂,那么,果皮成分能保护细胞免受紫外线辐射的伤害吗?有人对此进行了探究。
实验材料与用具:适宜浓度的大肠杆菌菌液、柚皮提取液、葡萄皮提取液、无菌水、已灭菌的大肠杆菌培养基(装在培养皿中)、接种环、紫外灯、恒温培养箱等。
实验步骤:
①取6块大肠杆菌培养基,编号为a、b、c、d、e、f。
②按下表配方配制接种液,然后使用接种环分别将菌种接种到6块培养基上。
|
培养基编号 |
接种液配方 |
|
a和d |
? +1mL无菌水 |
|
b和e |
3mL菌液+1mL柚皮提取液 |
|
c和f |
? |
③紫外线照射:将a、b、c三块已接种的培养基置于紫外灯正下方10cm处照射3min,然后立即用铝箔纸包住培养皿,放人37℃恒温培养箱中培养;……
④24h后,取出培养皿,观察、计数。
实验结果:
|
培养基编号 |
a |
b |
c |
d |
e |
f |
|
菌落数目 |
2 |
503 |
374 |
327 |
537 |
488 |
讨论:
(1)因紫外线辐射所产生的某些氧化产物,很可能是通过诱导__▲__而对细胞造成伤害的。
(2)a、d培养基接种液的配方是__▲__+1mL无菌水,c、f培养基接种液的配方是__▲__。
(3)在对a、b、c进行紫外灯照射时,对d、e、f的处理应该是__▲__。
(4)本实验的因变量是__▲__。
(5)通过对实验结果的分析,可以得出的初步结论是__▲__。
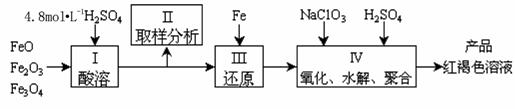
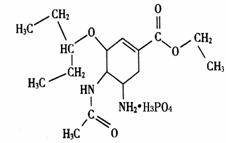
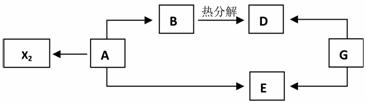
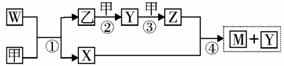
27.(15分)A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大,A元素原子的核外电子数、电子层数和最外层电子数均相等。B、C、D、E三种元素在周期表中相对位置如下左图,只有E元素的单质能与水反应生成两种酸。甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的若干种组成(只有M分子同时含有三种元素),其中甲、乙为非金属单质,W由A和C组成,分子中含有18个电子,X分子含有10个电子,它们之间的相互转化关系如下右图:
|
B |
C |
D |
|
|
|
|
|
E |
(1)E的单质与水反应的离子方程式为__▲__;
(2)W的分子式为__▲__ ; 元素A与B形成原子个数比为1∶1的相对分子质量最小化合物的结构式为__▲__;
(3)A、C、D三种元素组成一种强酸弱碱盐的化学式为__▲__,其水溶液中各种离子浓度由大到小顺序为__▲__;
(4)反应④的化学方程式为__▲__;
(5)W作火箭燃料时,氧化剂可以是Z,已知32 g W气体完全和Z气体反应生成乙和气态物质X,放出576.85 kJ热量,写出该反应的热化学方程式__▲__ 。
 C.若B是微生物,排到细胞外的代谢产物A最可能是初级代谢产物
C.若B是微生物,排到细胞外的代谢产物A最可能是初级代谢产物