江苏省海门市2009届高三第二次诊断性考试化学试题
(满分120分,考试时间100分钟)
第Ⅰ卷(选择题 共48分)
注意事项:
1.回答I卷前,考生务必在答题纸姓名栏内写上自己的姓名、考试科目、准考证号等,并用2B铅笔涂写在答题纸上。
2.每小题选出正确答案后,用2B铅笔把答题纸上对应题号的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案。不能答在试题卷上。
3.考试结束,将答题纸交回。
可能用到的相对原子质量:H-
Al-27 Si-28 Cl-35.5 K-39 Mn-55
一、选择题(本题包括8小题,每题3分,共24分。每小题只有一个选项符合题意)
1.下列有关说法不正确的是
A.可以利用电解的方法,从海水中获取淡水资源
B.以海水为原料,制备金属镁的过程中,一定发生了氧化还原反应
C.由铝土矿提取铝的过程中,不涉及置换反应
D.人类探月工程的目的之一是获取月球上的He-3资源
 2.下列各项中表达正确的是
2.下列各项中表达正确的是
 A.F原子结构示意图:
B.N2的结构式::N≡N:
A.F原子结构示意图:
B.N2的结构式::N≡N:
C.H、D、T表示同一种核素 D.CH4分子的球棍模型:
3.将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果。用数轴表示的下列化学知识中正确的是
A.平衡常数与转化率关系: B.分散系的分类:



 C.AlCl3和NaOH反应后铝元素的存在形式: D.Na与O2反应的产物:
C.AlCl3和NaOH反应后铝元素的存在形式: D.Na与O2反应的产物:


4.下列对化学反应的认识正确的是
A.化学反应过程中,分子的种类和数目一定发生改变
B.如果某化学反应的DH和DS均小于0,则反应一定能自发进行
C.化学反应过程中,一定有化学键的断裂和形成
D.放热反应的反应速率,一定比吸热反应的反应速率快
5.下图是化学能与电能相互转换的两套装置。对此两套装置的分析正确的是

A.两装置中,铁电极上均有气体产生
B.图2装置能将电能转化为化学能
C.石墨电极上发生的电极反应均为:2H++2e-=H2↑
D.随着反应的进行,两装置中电解质溶液的pH均增大
6.通过比较归纳可以加深对问题的认识。下列比较或归纳一定正确的是
A.酸性:H2SO4>H3PO4>H2SiO3 B.稳定性:NH3<PH3<AsH3
C.离子半径:阴离子>阳离子 D.熔沸点:离子化合物>共价化合物
7.利用下列实验装置完成相应的实验,能达到实验目的的是




 A.检验溶液中是否含有NaCl
B.除去乙醇中溶有的少量乙酸
A.检验溶液中是否含有NaCl
B.除去乙醇中溶有的少量乙酸
C.实验室中制取少量蒸馏水 D.用MnO2和浓盐酸制备Cl2
8.从矿物学资料查得,一定条件下自然界中存在如下反应:
14CuSO4+5FeS2+12 =7Cu2S+5FeSO4+12H2SO4,下列说法不正确的是
A. 中的物质是H2O B.上述产物中的SO42-,部分是氧化产物
C.CuSO4在反应中发生了还原反应 D.5mol FeS2发生反应,转移电子10 mol
二、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
9.NA代表阿伏加德罗常数的值,下列说法正确的是
A.分解H2O2制O2,每生成0.25 mol O2转移电子为NA
B.
C.将
D.铜的电解精炼时,电解池中每转移2 mol电子阳极上溶解的铜原子数等于NA
10.下列相对应的离子方程式正确的是
A、明矾溶于水后,溶液呈酸性: Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
B、用醋酸除去水垢中的碳酸盐: 2CH3COOH+CO32- 2CH3COO-+H2O+CO2↑
2CH3COO-+H2O+CO2↑
C、工业上电解食盐水制备Cl2: 2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D、用NaOH溶液吸收足量的SO2:2OH-+SO2 SO32-+H2O
SO32-+H2O
11.下列有关实验问题叙述正确的是
 A.测定中和热时,用环形铜质搅拌棒搅拌溶液,使测得的温度更准确
A.测定中和热时,用环形铜质搅拌棒搅拌溶液,使测得的温度更准确
B.利用烧杯、玻璃棒、量筒、容量瓶就可以配制2mol/L的硫酸溶液
C.用pH计测得某次雨水的pH为3.7
D.用标准浓度HCl滴定未知浓度NaOH溶液,中和滴定曲线如右图
12.符合下列各种条件的溶液中,各组离子可能大量共存的是
A.pH=0的溶液中: Na+、NH4+、CO32-、Cl-
B.Br-不能大量存在的溶液中: Mg2+、Ca2+、Cl-、NO3-
C.加入铝粉后能产生气体的溶液中: Cu2+、Ba2+、Cl-、NO3-
D.常温下水电离出的c(H+)=10-4的溶液中: Fe3+、K+、ClO-、SO42-
13.下列各种情况下,离子或分子浓度大小比较正确的是
A.物质的量浓度相等的(NH4)2SO4和(NH4)2SO3溶液中,NH4+浓度:前者大于后者
B.等物质的量浓度的CH3COONa和NaOH溶液中,阴离子总浓度:后者大于前者
C.将氨水和盐酸混合后,所得溶液中可能存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.将一定量CO2通入NaOH溶液后,所得溶液中一定存在:
c(Na+)+c(H+)=
14.除去下列物质中少量杂质的方法正确的是
A.除去SiO2中混有的Al2O3杂质,加入适量NaOH溶液,溶解过滤
B.除去KNO3晶体中混有的NaCl杂质,加水溶解、蒸发结晶、过滤
C.除去Na2CO3晶体中混有的NaHCO3杂质,置于坩埚中充分加热
D.除去NaCl溶液中混有的Na2SO4杂质,加入过量BaCl2,过滤
 15.同一物质在不同温度压强下,会呈现不同的状态。碘的三种状态与温度、压强的关系如右图所示。根据图中信息得出的结论不正确的是
15.同一物质在不同温度压强下,会呈现不同的状态。碘的三种状态与温度、压强的关系如右图所示。根据图中信息得出的结论不正确的是
A.对碘固体加热,碘将从固态直接变成气态
B.在P0 kPa、T0 K时,碘的三种状态可以同时存在
C.在P1 kPa、T1 K时,碘以气态形式存在
D.在P1 kPa时,将碘蒸气降温,可以看到碘蒸气变成液态
16.将总物质的量为n mol的钠和铝(其中钠的物质的量分数为x),投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V L。下列关系式中正确的是
A.x= B.0<x≤0.5
B.0<x≤0.5
C.V=33.6n(1-x) D.11.2n<V≤22.4n
第二卷(非选择题 共72分)
三.(本题包括2小题,共20分)

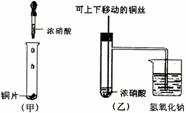 17.( 8分)下图(甲)是课本中验证铜和浓硝酸反应的装置,图(乙)、图(丙)是某校师生改进后的装置:
17.( 8分)下图(甲)是课本中验证铜和浓硝酸反应的装置,图(乙)、图(丙)是某校师生改进后的装置:
(1)写出铜和浓硝酸反应的离子方程式 。
(2)和图(乙)装置相比,甲装置的缺点是 。
(3)为了进一步验证NO2和水的反应,某学生设计了图(丙)装置,对a、b、c三只弹簧夹操作:先关闭弹簧夹 ,再打开弹簧夹 ,才能使NO2气体充满试管②。
(4)图(丙)装置中,当气体充满试管②后,将铜丝提起与溶液脱离,欲使烧杯中的水进入试管②应如何操作 。
18.(12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
实 验 步 骤
现 象
结 论
①分别取等体积的2 mol/L硫酸于试管中;
②分别投入大小、形状相同的Cu、Fe、Mg。
反应快慢:
Mg>Fe>Cu
反应物的性质越活泼,反应速率越快。
(1 )该同学的实验目的是________________________________;
)该同学的实验目的是________________________________;
要得出正确的实验结论,还需控制的实验条件是________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图
装置进行定量实验。完成该实验应选用的实验药品是______;
应该测定的实验数据是____________________________。
实验二:已知2KMnO4+5H
(1)针对上述实验现象,某同学认为KMnO4与H
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是____
A、硫酸钾 B、硫酸锰 C、氯化锰 D、水
四.(本题包括2小题,共20分)
19.(10分)在某个容积为
mA(g)+nB(g) pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。



(1)据图1所示,反应开始至达到平衡时,用D表示该反应速率为_____mol/L?min;
(2)该反应的化学平衡常数K的数值为_________________(保留至两位小数);
(3)反应达到平衡后,第7 min时:
①若升高温度,D的浓度变化最可能的是_____(用图2中a~c的编号回答);
②若将容器的容积压缩为原来一半,请在图3中画出7 min后D浓度变化情况。
(4)在T℃时,相同容器中,若开始时加入0.2 mol A 、0.8 mol B 、0.9 mol D 、0.5 mol E反应,达到平衡后,A的浓度范围为_______________________。
(5)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是_______
A、化学反应速率理论可指导怎样在一定时间内快出产品;
B、有效碰撞理论可指导怎样提高原料的转化率;
C、勒夏特列原理可指导怎样使用有限原料多出产品;
D、正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益。
20.(10分)已知A为常见金属,常温下X、E、F为气体,C为液体。B是一种盐,受热易分解,冷却时分解产物又能化合生成B,B在工农业生产中有着广泛的用途。有关物质之间的转化关系如下图(其中有些反应的条件及部分生成物被略去):

请回答下列问题:
(1)写出物质B的电子式 ;
(2)比较①~⑦七个反应,请归纳它们的共同特点是 ;
(3)写出反应⑦的化学方程式 ;
(4)写出过量A与H浓溶液反应的离子方程式 ;
(5)D是实验中常用的物质,检验D是否变质的方法是:
。
五.(本题包括1小题,共12分)
21.(12分)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为__________;
(2)写出与H2O分子互为等电子体的微粒__________。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是______(请用相应的编号填写)





A B C D E
 (5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
六.(本题包括1小题,共10分)
22.(10分)科学家预测“氢能”将是未来最理想的新能源。请回答下列问题:
(1)实验测得,
A.2H2(g) + O2(g) = 2H2O(l); △H =-142.9 kJ/mol
B.H2(g) + 1/2O2(g) = H2O(l); △H =-285.8 kJ/mol
C.2H2(g) + O2(g) = 2H2O(l);△H =-571.6 kJ/mol
D.H2(g) + 1/2O2(g) = H2O(g);△H = -285.8 kJ/mol
(2)根据“绿色化学”的思想,为了制备H2,某化学家设计了下列化学反应步骤:
①CaBr2+H2O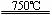 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg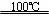 HgBr2+H2↑
HgBr2+H2↑
③HgBr2+ HgO
HgO 2Hg+O2↑
2Hg+O2↑
上述过程的总反应可表示为 。
(3)利用核能把水分解,制出氢气,是目前许多国家正在研究的课题。下图是国外正在研究中的一种流程(硫―碘热循环法),其中用了过量的碘。

请写出反应①的化学方程式: 。
用硫―碘热循环法制取氢最大的优点是 。
(4)也有人认为利用氢气作为能源不太现实。你的观点呢?请说明能够支持你的观点的两点理由 。
七.(本题包括1小题,共10分)
23.(10分)称取
(1)如果配制上述500 mL浓HCl,则需标准状况下HCl气体的体积为 L。
(2)如果以KMnO4的分解率为横坐标,收集到气体的物质的量为纵坐标,请在下图中分别作出O2和Cl2物质的量与分解率x之间的关系曲线。

(3)当a=0.016 mol时,收集到Cl2的物质的量为______。
(4)当a+b=0.09时,计算上述加热分解后残留固体的质量。
一.选择题(本题包括8小题,每小题3分,共24分)
题号
1
2
3
4
5
6
7
8
答案
A
D
B
C
B
A
C
D
二.选择题(本题包括8小题,每小题3分,共24分)
题号
9
10
11
12
13
14
15
16
答案
B
AC
C
BC
AD
C
AD
D
三.(本题包括2小题,共20分)
17.(共8分)
(1)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O (2分)
(2)①不易控制反应。②产生有毒气体,造成污染环境。(2分)
(3)c; a、b。(2分)
(4)关闭a, b,打开c (1分) 用手捂住(热水、热毛巾、加热)试管② (1分)
(合理答案均给分)
18.(每空2分,共12分)
实验一:(1)反应物本身的性质对反应速率的关系;(2分)
温度相同;(2分)
(2)Mg(或Fe)和0.5mol/L硫酸和2mol/L硫酸;(2分)
测定一定时间产生气体的体积(或者测定一定体积的气体所需时间);(2分)
实验二:(1)催化剂(或硫酸锰或Mn2+的催化作用);(2分)
 (2)B
(2分)
(2)B
(2分)
四.(本题包括2小题,共20分)
19.(每空2分,共10分)
(1)0.1;(2)1.69;
(3)①c;②(参看右图)
(4)0<c(A)<0.2mol/L;(5)B
20.(每空2分,共10分)
(1) (2分)
(2分)
(2)均为氧化还原反应 (2分)
(3)3Fe+ 4H2O  Fe 3O4+4H2↑
(2分)
Fe 3O4+4H2↑
(2分)
(4)Fe+4H++2NO3-=Fe2++2NO2↑+2 H2O (2分)
(5)取少量样品于试管中,加入KSCN溶液,如果出现红色,说明变质;反之,没有变质 (2分)
五.(本题包括1小题,共12分)
21.(共12分)
(1)1S22S22P6;(2分)(2)H2S或NH2-;(2分)
(3)A;(2分)(4)BC;(2分)(5)20; (2分)
(6)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
六.(本题包括1小题,共10分)
22.(共10分)
(1)B (2分)
(2)2H2O 2H2↑+O2↑
(2分)
2H2↑+O2↑
(2分)
(3) SO2+I2+2H2O 2HI+H2SO4 (2分)
2HI+H2SO4 (2分)
SO2和I2可循环使用,无污染。 (2分)
(4)不现实,理由是现有的制取氢气方法耗能大,制取的成本太高,另外是氢气的熔沸点太低,给储存和运输带来困难。(或:现实,制取氢气用水为原料,来源丰富;氢气燃烧的产物是水,不会给环境带来任何污染等。) (2分)
 七.(本题包括1小题,共10分)
七.(本题包括1小题,共10分)
23.(10分)
(1)134.4;
(2) (参看右图);
(3)0.068mol;
(4)
说明:本试卷中其他合理答案同样给分。