网址:http://m.1010jiajiao.com/timu_id_576644[举报]
一.选择题(本题包括8小题,每小题3分,共24分)
题号
1
2
3
4
5
6
7
8
答案
A
D
B
C
B
A
C
D
二.选择题(本题包括8小题,每小题3分,共24分)
题号
9
10
11
12
13
14
15
16
答案
B
AC
C
BC
AD
C
AD
D
三.(本题包括2小题,共20分)
17.(共8分)
(1)Cu+4H++2NO3-=Cu2++2NO2↑+2H2O (2分)
(2)①不易控制反应。②产生有毒气体,造成污染环境。(2分)
(3)c; a、b。(2分)
(4)关闭a, b,打开c (1分) 用手捂住(热水、热毛巾、加热)试管② (1分)
(合理答案均给分)
18.(每空2分,共12分)
实验一:(1)反应物本身的性质对反应速率的关系;(2分)
温度相同;(2分)
(2)Mg(或Fe)和0.5mol/L硫酸和2mol/L硫酸;(2分)
测定一定时间产生气体的体积(或者测定一定体积的气体所需时间);(2分)
实验二:(1)催化剂(或硫酸锰或Mn2+的催化作用);(2分)
 (2)B
(2分)
(2)B
(2分)
四.(本题包括2小题,共20分)
19.(每空2分,共10分)
(1)0.1;(2)1.69;
(3)①c;②(参看右图)
(4)0<c(A)<0.2mol/L;(5)B
20.(每空2分,共10分)
(1) (2分)
(2分)
(2)均为氧化还原反应 (2分)
(3)3Fe+ 4H2O  Fe 3O4+4H2↑
(2分)
Fe 3O4+4H2↑
(2分)
(4)Fe+4H++2NO3-=Fe2++2NO2↑+2 H2O (2分)
(5)取少量样品于试管中,加入KSCN溶液,如果出现红色,说明变质;反之,没有变质 (2分)
五.(本题包括1小题,共12分)
21.(共12分)
(1)1S22S22P6;(2分)(2)H2S或NH2-;(2分)
(3)A;(2分)(4)BC;(2分)(5)20; (2分)
(6)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
六.(本题包括1小题,共10分)
22.(共10分)
(1)B (2分)
(2)2H2O 2H2↑+O2↑
(2分)
2H2↑+O2↑
(2分)
(3) SO2+I2+2H2O 2HI+H2SO4 (2分)
2HI+H2SO4 (2分)
SO2和I2可循环使用,无污染。 (2分)
(4)不现实,理由是现有的制取氢气方法耗能大,制取的成本太高,另外是氢气的熔沸点太低,给储存和运输带来困难。(或:现实,制取氢气用水为原料,来源丰富;氢气燃烧的产物是水,不会给环境带来任何污染等。) (2分)
 七.(本题包括1小题,共10分)
七.(本题包括1小题,共10分)
23.(10分)
(1)134.4;
(2) (参看右图);
(3)0.068mol;
(4)
说明:本试卷中其他合理答案同样给分。
|
已知:H2(g)+O2(g)=H2O(l);ΔH=-285.8 kJ·mol-1 CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1 现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 kJ,则原混合气体中H2与CH4的物质的量之比是 | |
| [ ] | |
A. |
1∶1 |
B. |
2∶3 |
C. |
1∶4 |
D. |
1∶3 |
已知反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g) △H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4。
H2(g)+CO2(g) △H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4。
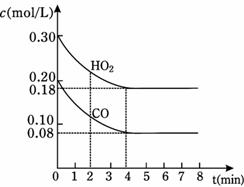
(1)850℃时在一体积为10 L的恒容密闭容器中,通入一定量的CO和H2O(g),CO和H2O(g)浓度变化如右图所示,下列说法正确的是 (填序号)。
A.达到平衡时,反应体系最终会放出49.44kJ热量;
B.第4min时,混合气体的平均相对分子质量不再变化,可判断已达到平衡;
C.第6min时,若升高温度,反应平衡常数会增大; 850℃时物质浓度的变化
D.第8min时,若充入CO,会导致v(正)>v(逆),平衡向正反应方向移动。
(2)850℃时,若在容积为2L的密闭容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2和x mol H2。若要使上述反应开始时向正反应方向进行,则x应满足的条件是 。
(3)如将H2与CO2以4∶1的体积比混合,在适当的条件下可制得CH4。已知:
CH4(g) + 2O2(g)=CO2 (g)+ 2H2O (1) ΔH1=-890.3 kJ/mol
H2(g)+![]() O2(g)=H2O (1) ΔH2=-285.8 kJ/mol
O2(g)=H2O (1) ΔH2=-285.8 kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是 。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。负极反应式为 ,正极反应式为 。
查看习题详情和答案>>
B.1mol H2完全燃烧生成液态水时放出285.8kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.上述热化学方程式可表示为H2(g)+1/2O2(g)=H2O(l);△H=-285.8 kJ·mol-1
(1)已知:在1×105Pa条件下,氢气的标准燃烧热是285.8 kJ·mol-1,下列热化学方程式正确的是 ( )
A.H2O(g)=H2(g)+1/2O2(g) ΔH=+285.8kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l) ΔH=—517.6kJ·mol-1
C.H2(g)+1/2 O2(g)=H2O(g) ΔH=—285.8kJ·mol-1-
D.2H2(g)+O2(g)=2H2O(l) ΔH=+517.6J·mol-1
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
① P4(s,白磷)+ 5O2(g)=P4O10(s); ΔH=—2983.2kJ·mol-1
② P(s,红磷)+ 5/4 O2 (g) =1/4 P4O10(s) ΔH=—738.5kJ·mol-1-
则白磷转化为红磷的热化学方程式_________________________________。相同的状况下,能量较低的是_________;白磷的稳定性比红磷___________(填“高”或“低”)
查看习题详情和答案>>(1)已知:在1×105Pa条件下,氢气的标准燃烧热是285.8 kJ·mol-1,下列热化学方程式正确的是 ( )
A.H2O(g)=H2(g)+1/2O2(g) ΔH=+285.8kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l) ΔH=—517.6kJ·mol-1
C.H2(g)+1/2 O2(g)=H2O(g) ΔH=—285.8kJ·mol-1-
D.2H2(g)+O2(g)=2H2O(l) ΔH=+517.6J·mol-1
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
① P4(s,白磷)+ 5O2(g)=P4O10(s); ΔH=—2983.2kJ·mol-1
② P(s,红磷)+ 5/4 O2 (g) =1/4 P4O10(s) ΔH=—738.5kJ·mol-1-
则白磷转化为红磷的热化学方程式_________________________________。相同的状况下,能量较低的是_________;白磷的稳定性比红磷___________(填“高”或“低”)
查看习题详情和答案>>