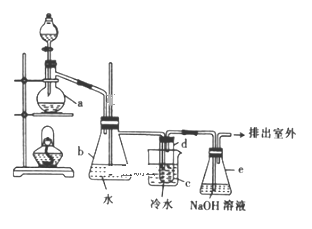
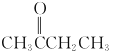【题目】某分子的结构如图所示(-R 为烃基),其中 A、B、D 三种元素位于元素周期表中同一族的三个相邻的周期,A 的非金属性大于 B。D 与 G 形成的 DG3 在工业上可用于漂白和杀菌消毒。A 与 G 形成的 AG3 可完全水解,其水解的产物之一 H3AO3 常用作塑料件镀金属的还原剂。
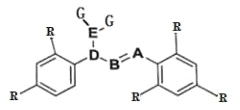
(1)具有未成对电子的原子或分子具有磁性。D 的某种氧化物 D2O4 的磁性大小与温度呈正相关关系,即磁性是温度的增函数。则 D2O4 ![]() 2DO2,ΔH______0(填“>”“<”或“=”)。
2DO2,ΔH______0(填“>”“<”或“=”)。
(2)DG3 用于杀菌消毒与 HGO 相比,DG3 可大大延长杀菌消毒的时间,试从反应速率理论和平衡移动理论两者中选择一个,解释其原因____________________________。
(3)无机含氧酸中的非羟基氢不能发生电离。H3AO3 分子中 A 原子最外层的电子都参与了共价键的形成,试用方程式表示 H3AO3 的正盐溶液呈碱性的原因_____。
(4)液氨中因存在2NH3(1) ![]() NH4++NH2-可导电,液态 D2O4 中也存在 D2O4
NH4++NH2-可导电,液态 D2O4 中也存在 D2O4![]() DO++DO3-,上述两个过程的本质区别为___________。
DO++DO3-,上述两个过程的本质区别为___________。
(5)T℃时,在一体积为 VL 的密闭容器中放入一定量的 ACl5 固体,按下式发生反应:ACl5(s)![]() ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:
ACl3(g)+Cl2(g),ΔH>0。测得容器内气体的压强变化如下表:
时间 t/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | ∞ |
总压 P/kPa | 0 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 | 5.0 | 5.0 |
上述条件下,以分压表示的平衡常数 Kp=_____(kPa)2(计算结果保留两位小数); 若保持温度不变,30s 时给容器加压,达新平衡后,容器内的总压将_____(填“升高”、“降低”或“不变”);若将容器换成绝热容器,加压后容器内的总压将_____(填“升高”、“降低”或“不变”)。