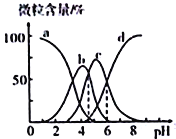
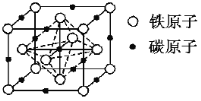
【题目】下表是![]() 时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是![]()
化学式 | AgCl |
|
| HClO |
|
Ksp或Ka |
|
|
|
|
|
A.相同浓度![]() 和NaClO的混合液中,各离子浓度的大小关系是
和NaClO的混合液中,各离子浓度的大小关系是![]()
B.向![]() 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至![]() :
:![]() :9,此时溶液
:9,此时溶液![]()
C.碳酸钠溶液中滴加少量氯水的离子方程式为![]()
D.向浓度均为![]() 的KCl和
的KCl和![]() 混合液中滴加
混合液中滴加![]() 的
的![]() 溶液,
溶液,![]() 先形成沉淀.
先形成沉淀.
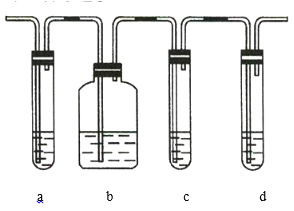
【题目】下列有关实验操作与相应结论都正确的是![]()
选项 | 实验操作及现象 | 实验结论 |
A | 取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润蓝色石蕊试纸变红. | 可证明晶体的成分中含有 |
B | Z、W两试管中分别盛有pH和体积相同的盐酸和醋酸溶液,同时分别投入质量大小、形状相同的少量锌粒,Z中产生气体速率快 | Z中盛放的是醋酸 |
C | 向尿液中加入新制 | 说明尿液中不含有葡萄糖 |
D | 某待测液先滴入氯水无明显现象,后滴入硫氰化钾溶液出现血红色 | 该待测液中一定含有 |
A.AB.BC.CD.D
【题目】![]() 在工业、农业等方面有广泛的应用,工业上可由高铁菱锰矿(主要成分为
在工业、农业等方面有广泛的应用,工业上可由高铁菱锰矿(主要成分为![]() ,含有
,含有![]() 、
、![]() 、
、![]() 、
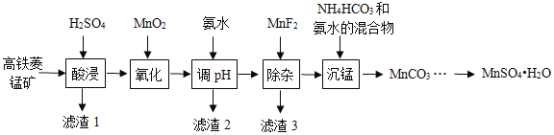
、![]() 等杂质)制备,部分工艺流程如图所示:
等杂质)制备,部分工艺流程如图所示:
相关金属离子生成氢氧化物沉淀的![]() (开始沉淀的
(开始沉淀的![]() 按离子浓度为
按离子浓度为![]() 计算):
计算):
金属离子 |
|
|
|
|
|
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“氧化”时发生反应的离子方程式为______________。
(2)“调![]() ”范围至5~6,得到滤渣2的主要成分除
”范围至5~6,得到滤渣2的主要成分除![]() 外还有_____________。
外还有_____________。
(3)“除杂”过程中加入![]() 的目的是______。
的目的是______。
(4)“沉锰”过程中发生反应的化学方程式为______。
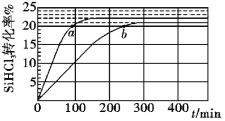
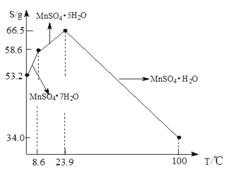
(5)![]() 在水中的溶解度与温度关系如图。由
在水中的溶解度与温度关系如图。由![]() 获得较纯净的
获得较纯净的![]() 晶体的方法是:将
晶体的方法是:将![]() 溶于适量的稀硫酸,控制温度在
溶于适量的稀硫酸,控制温度在![]() 之间蒸发结晶,______,得到
之间蒸发结晶,______,得到![]() 晶体,洗涤、烘干。晶体通常采用减压烘干的原因是______。
晶体,洗涤、烘干。晶体通常采用减压烘干的原因是______。
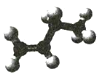
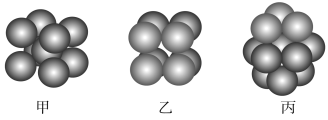
【题目】已知表中是某些有机物的模型图,根据要求回答下列问题:
有机物 | 甲 | 乙 | 丙 |
模型 |
|
|
|
(1)甲的分子式是___________________,其一氯代物有___________________种。
(2)写出乙与![]() 的
的![]() 溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
溶液发生反应的化学方程式:______________________________________,该反应的反应类型是___________________。
(3)丙的摩尔质量为![]() ,则用苯制备该物质时的催化剂是___________________。
,则用苯制备该物质时的催化剂是___________________。
【题目】化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过反应3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答下列问题:
(1)与(HB=NH)3互为等电子体的分子为________(填分子式)
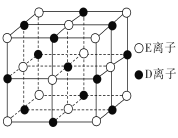
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的结构类似,则其晶体中每个硼原子与____个氮原子相连,每个氮原子与_____个硼原子相连。
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上采用LiAlH4和BF3在乙醚介质中反应制得乙硼烷(B2H6),同时生成另外两种产物。该反应的化学方程式为___________。
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
化学键 | B—H | B—O | B—B |
键能(kJ·mol-1) | 389 | 561 | 293 |
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化合物,其原因为____________。
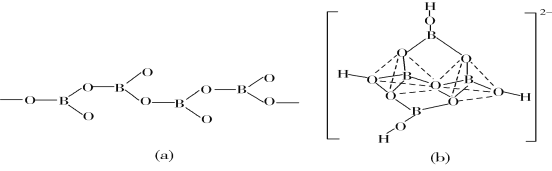
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式。图(a)为一种无限长单链结构的多硼酸根,其化学式为________;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型为________。